
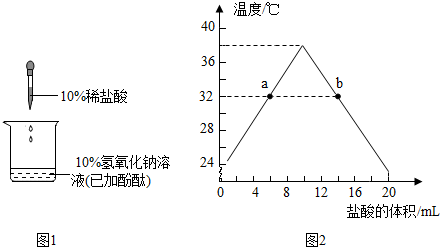
分析 (1)根据酚酞试液在碱性溶液中的变色情况来分析;
(2)根据稀盐酸能与氢氧化钠发生中和反应来分析;
(3)根据无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,结合当溶液的pH等于7时,呈中性,进行分析解答.
(4)根据到达b点的温度变化来分析;
(5)根据氢氧化钠的性质来分析.
解答 解:(1)氢氧化钠溶液是一种碱性溶液能使无色酚酞试液变红色;
故填:红;
(2)随着滴入稀盐酸,氢氧化钠与稀盐酸发生中和反应生成氯化钠和水,盐酸显酸性,随着盐酸的滴加,溶液的碱性减弱,酸性增强,pH变小;
故填:减小;NaOH+HCl=NaCl+H2O;
(3)借助无色酚酞试液观察反应进程,当反应获得的溶液PH恰好为7时,溶液显中性,此时溶液由红色变为无色.
故填:溶液由红色变为无色.
(4)b点的温度是由高到低的趋势,说明是中和反应恰好完成后,继续滴加稀盐酸到过量,
故填:酸性,因为是溶液的温度由高到降低;
(5)A.在实验室中不能品尝试剂的味道;
B.此液体具有腐蚀性,不能用手直接接触;
C.往烧杯中再滴加少量氢氧化钠溶液并观察瞬间溶液颜色变化,若先变红,后变无色,证明其中没有氢氧化钠.
故选C.
点评 本题考查了中和反应过程中的热量变化,完成此题,可以依据已有的知识以及图象进行.


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:选择题
| A. | 相对原子质量为235克 | B. | 电子数为92 | ||
| C. | 核电荷数为92 | D. | 相对原子质量为235 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在空气中剧烈燃烧,火星四射,生成一种黑色固体 | |
| B. | 木炭在氧气中燃烧,发出白光,放出热量 | |
| C. | 水通电一段时间后,正极与负极产生的气体体积比约为1:2 | |
| D. | 将铁钉放在硫酸铜溶液中,铁钉上有红色固体附着,蓝色溶液逐渐变为浅绿色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 1 | 2 | 3 | 4 | 5 | 6 | |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO (质量比l:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
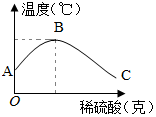 学习酸碱反应时,很多同学对其产生探究兴趣.
学习酸碱反应时,很多同学对其产生探究兴趣.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com