
| A. | CH4 | B. | C2H6 | C. | C2H2 | D. | C3H8 |
分析 根据给出的限制条件可知,因为最后容器内几乎是真空,说明可以剩余气体,但是很少,应该理解为甲烷或者是氧气,生成的二氧化碳的分子数和剩余气体的分子数和为可燃物和氧气的分子数的和的一半.剩余气体越少,真空度越高.至于“容器内气体分子是反应前的一半”,不能理解为水的分子水一定就是就是反应物分子的一半.
解答 解:因为最后容器内几乎是真空,说明可以剩余气体,但是很少,由于不考虑生成一氧化碳,应该理解是氧气,最近接近真空,则剩余气体与原气体总体积相比,越小真空程度越大.生成的二氧化碳的分子数和剩余气体的分子数和为可燃物和氧气的分子数的和的一半. 逐一配平化学方程式,分析可燃物和氧气的分子数的和,对比二氧化碳的分子数即可:
假设每个反应剩余气体都是1体积,从分子的角度理解为1分子.
A、CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,可燃物和氧气分子数的和为3,加上剩余1分子氧气,反应前的总分子数为4分子,而二氧化碳和剩余氧气分子总数为2,所以为一半,但是当经过氢氧化钠溶液吸收后,剩余体积为1,也就是为四分之一;
B、2C2H6+7O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+6H2O,可燃物和氧气分子数的和为9,加上剩余1分子氧气,反应前的总分子数为10分子,而二氧化碳和剩余氧气分子总数为5,所以为一半,但是当经过氢氧化钠溶液吸收后,剩余体积为1,也就是为十分之一;
C、2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,可燃物和氧气分子数的和为7,加上剩余1分子氧气,反应前的总分子数为8分子,而二氧化碳和剩余氧气分子总数为5,不到一半.错误;
D、C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O,可燃物和氧气分子数的和为6,加上剩余1分子氧气,反应前的总分子数为7分子,而二氧化碳和剩余氧气分子总数为4,超过了一半.错误;
AB对比,真空度更高的是B.
故选:B.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
| A. | 胃液(0.8~1.5) | B. | 尿液(5.0~7.0) | C. | 血液(7.4~7.5) | D. | 小肠液(7.8~8.0) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
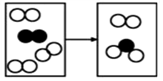
 B.
B. C.
C.
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 无需变动 | B. | 减少流量 | C. | 加大流量 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
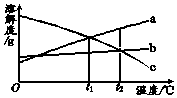 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )| A. | 原饱和溶液中,溶质的质量分数a=c>b | |
| B. | 恢复至t1℃时,析出溶质的质量a=c>b | |
| C. | 恢复至t1℃时,三种溶液都是饱和溶液 | |
| D. | 若继续升温至t2℃,三种溶液都是饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | X | Y | Z | W |
| 反应前的质量/g | 10 | m | 8 | 7 |
| 反应后的质量/g | 2 | 3 | 30 | 25 |
| A. | m的数值为32 | |
| B. | 参加反应的X与Y的质量比为1:4 | |
| C. | 若W为水,则X或Y必定为酸或碱 | |
| D. | 若X为化合物,Y为单质,则Z和W中也一定有一种单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2% | B. | 4% | C. | 10% | D. | 19.6% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合理使用化肥,爱护土地 | |
| B. | 节约、珍惜水资源 | |
| C. | 将公共交通工具作为出行首选,使用清洁能源 | |
| D. | 尽力开采金属矿物,推广使用金属制品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com