
| A. | 水分子是由氢原子和氧原子构成的,氢原子和氧原子能保持水的化学性质 | |
| B. | 化学反应过程的实质是分子破裂原子重新组合 | |
| C. | 将水加热变成水蒸气,体积变大,是因为水分子体积变大 | |
| D. | 花香四溢主要是因为分子间有间隔 |
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:初中化学 来源: 题型:选择题
| A. | 是一种有机物 | B. | 由碳、氢、氧元素组成 | ||
| C. | 碳、氢、氧元素的质量比是1:2:1 | D. | 相对分子质量为30 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应:
1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
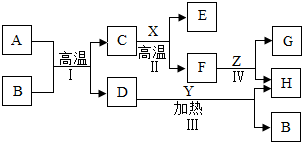 (1)X、Y、Z、W、R是初中化学常见的五种元素,X的单质是密度最小的气体,Y的一种单质是天然存在的最硬物质,Z是地壳中含量最多的元素,W的原子序数为11,R的原子结构示意图为
(1)X、Y、Z、W、R是初中化学常见的五种元素,X的单质是密度最小的气体,Y的一种单质是天然存在的最硬物质,Z是地壳中含量最多的元素,W的原子序数为11,R的原子结构示意图为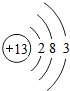 ,请回答下列问题:①X阳离子的离子结构示意图为
,请回答下列问题:①X阳离子的离子结构示意图为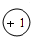 ,W离子的离子符号为Na+;
,W离子的离子符号为Na+;查看答案和解析>>
科目:初中化学 来源: 题型:解答题
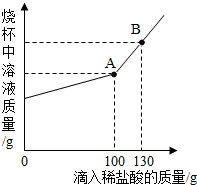
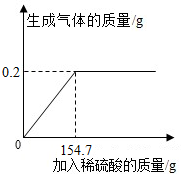 学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”),为进一步定量分析黄铜的成分,某同学进行了如下实验,称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生成的气体与所加稀硫酸的质量关系如图所示,求:
学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”),为进一步定量分析黄铜的成分,某同学进行了如下实验,称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生成的气体与所加稀硫酸的质量关系如图所示,求:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用酚酞鉴别食盐水和稀醋酸 | B. | 用水鉴别生石灰和石灰石 | ||
| C. | 用燃着的木条鉴别空气和二氧化碳 | D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 问题 | 对问题的回答 |
| A | 吹灭蜡烛时产生的白烟是什么? | 主要成分是烛油蒸气 |
| B | 火焰为什么向上? | 热气流上升,形成对流 |
| C | 火焰明亮的原因是什么? | 与火焰中有碳颗粒有关,碳颗粒会影响火焰明亮程度 |
| D | 火焰不同部位温度高低如何比较? | 用一张纸在火焰中心一掠,观察纸上留下的火痕特点 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
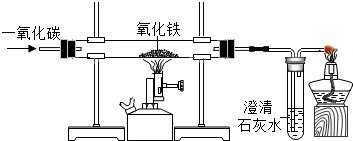
| 物质 性质 | Fe | Fe2O3 | FeO | Fe3O4 |
| 颜色 | 黑色 | 红色 | 黑色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com