
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g | NaCl | 35.7 | 36.0 | 36.6 | 37.3] | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
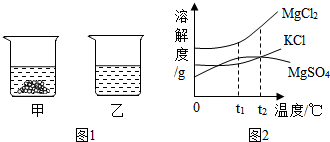
分析 (1)①根据氯化钠常用于配制0.9%的生理盐水,生理盐水中溶质为氯化钠进行解答;
②根据溶液稀释前后溶质质量不变解答;
③根据根据NaCl、NH4Cl在40℃时的溶解度计算分析加入的物质;
④根据氯化铵和氯化钠在不同温度下的溶解度分析判断有关的说法;
(2)根据过滤时玻璃棒的作用是引流解答;根据蒸发时玻璃棒的作用是搅拌,防止局部过热造成液滴飞溅解答;
(3)根据某一温度时物质溶解度的比较方法,溶解度越大,溶质的质量分数越大考虑.
解答 解:(1)①氯化钠常用于配制0.9%的生理盐水,生理盐水中溶质为氯化钠;
②溶液稀释前后溶质质量不变,需要加入蒸馏水的质量=$\frac{180g×10%}{0.9%}$-180g=1820g;
③由氯化铵和氯化钠在不同温度下的溶解度可可知,在40℃时,氯化铵和氯化钠的溶解度分别是45.8g、36.6g,由图示可知,乙烧杯中的物质完全溶解,则乙烧杯的物质为氯化铵.
④A、由于在40℃时,氯化铵的溶解度是45.8g,所以,40℃时,向盛有45g NH4Cl和NaCl的烧杯中,加入100g水,充分溶解后,烧杯乙中溶液是不饱和溶液.故A正确;
B、由于在40℃时,氯化钠的溶解度是36.6g.所以,40℃时,向盛有45g氯化钠的烧杯中,加入100g水,充分溶解后,烧杯甲中溶液是饱和溶液,只能溶解36.6g,甲中溶质的质量分数为:$\frac{36g}{100g+36g}×$100%═26.9%.故B错误;
C、由氯化钠在不同温度下的溶解度可知,在100℃,氯化钠的溶解度是39.8g,所以,升高温度不可能将烧杯甲中固体全部溶解.故C错误;
D、由于在20℃氯化铵的溶解度是37.2g,所以,将烧杯乙中溶液降温至20℃时,溶液中溶质的质量分数一定减小.故D正确.
(2)过滤时玻璃棒的作用是引流;蒸发时玻璃棒的作用是搅拌,防止局部过热造成液滴飞溅;
(3)虽然是升温到t2℃,但是由于没有加入溶质,所以对氯化镁和氯化钾质量分数计算依旧要按照t1℃时计算,而硫酸镁温度变化了,溶解度降低了,但是依旧比t1℃的氯化钾的溶解度大,所以从t1℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t1℃时它们的溶解度小到大顺序是KCl溶液、MgSO4溶液、MgCl2溶液;根据饱和溶液溶质的质量分数=$\frac{溶解度}{100g+溶解度}×$100%可知,溶解度越大,饱和溶液溶质的质量分数,故3种溶液溶质的质量分数由小到大的顺序是KCl溶液、MgSO4溶液、MgCl2溶液.
答案:
(1)①氯化钠 ②1820 ③氯化铵 ④AD
(2)引流 搅拌,防止局部过热造成液滴飞溅
(3)KCl溶液、MgSO4溶液、MgCl2溶液.
点评 此题考查溶解度知识的具体应用,对学生深入理解溶解度的概念有一定帮助,同时也复习了有关混合物分离的一些常识性的基础知识.


 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 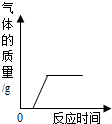 在久置的NaOH溶液中滴加盐酸 | |
| B. |  锌加入足量的稀硫酸中 | |
| C. |  往Na2SO4和HCl的混合溶液中加入Ba(OH)2溶液 | |
| D. |  向pH=9的NaOH溶液中不断加水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
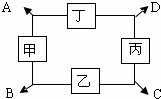 如图中的甲、乙、丙、丁是初中化学常见的四种不同类别的物质,相邻两种物质可发生化学反应,生成A、B、C、D四种物质(部分生成物已略去).其中乙是应用最广泛的金属,丙是一种蓝色溶液,B为硫酸盐,C为单质.请回答下列问题:
如图中的甲、乙、丙、丁是初中化学常见的四种不同类别的物质,相邻两种物质可发生化学反应,生成A、B、C、D四种物质(部分生成物已略去).其中乙是应用最广泛的金属,丙是一种蓝色溶液,B为硫酸盐,C为单质.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com