
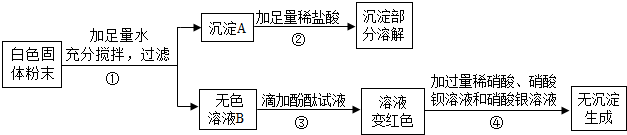
分析 根据硫酸根离子会与钡离子结合生成难溶于酸的硫酸钡沉淀,铜离子和氢氧根离子生成的氢氧化铜沉淀可以溶于酸,氯离子和银离子生成的氯化银沉淀难溶于酸进行分析.
解答 解:(1)取白色固体加入足量的水溶解、过滤后得到沉淀A和无色溶液B,在沉淀A中,加入足量的稀盐酸,沉淀部分溶解,硫酸铜和氢氧化钠会生成氢氧化铜沉淀和硫酸钠,氢氧化铜沉淀会溶于盐酸,硫酸铜和硝酸钡反应生成硫酸钡沉淀和硝酸铜,硫酸钡沉淀不溶于酸,所以白色固体中一定存在硫酸铜、氢氧化钠、硝酸钡;在无色溶液B中,滴加酚酞试液,溶液变红,说明B溶液中存在氢氧化钠,向溶液中依次加入过量的稀硝酸、硝酸钡溶液和适量硝酸银溶液,无沉淀生成,氯化钠和硝酸银会生成氯化银沉淀和硝酸钠,氯化银沉淀难溶于硝酸,所以白色固体中不存在氯化钠,白色固体中是否存在硫酸钠,对实验现象不会造成影响,所以白色固体中可能含有硫酸钠,所以原白色固体中一定含有:CuSO4、Ba(NO3)2、NaOH,一定没有:NaCl,可能含有:Na2SO4;
故答案为:CuSO4、Ba(NO3)2、NaOH;Na2SO4;
(2)无色酚酞在碱性溶液中显红色,在无色溶液B中,滴加酚酞试液,溶液变红,结合(1)中的分析,说明B溶液中含有过量的氢氧化钠、反应生成的硝酸钠;
故答案为:NaOH、NaNO3;
(3)步骤②沉淀溶解时氢氧化铜和盐酸反应产生氯化铜和水,故反应的方程式为:Cu(OH)2+2HCl═CuCl2+2H2O.
点评 本题为框图式推断题,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
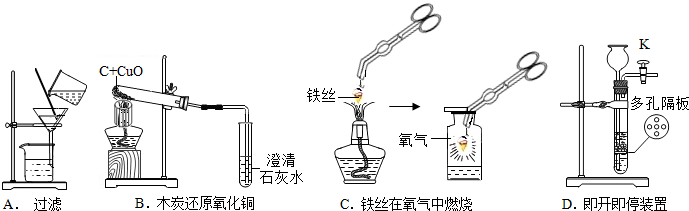
| A. | 铁丝在氧气中燃烧,火星四射 | B. | 红磷在空气中燃烧产生大量白烟 | ||
| C. | 镁条在空气中燃烧发出耀眼的白光 | D. | 硫粉在氧气中燃烧产生淡蓝色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
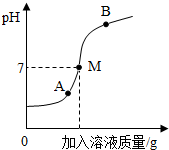 如图是氢氧化钠溶液与稀硫酸反应时,溶液的pH变化曲线图.下列说法正确的是( )
如图是氢氧化钠溶液与稀硫酸反应时,溶液的pH变化曲线图.下列说法正确的是( )| A. | 该实验是将稀硫酸滴入氢氧化钠溶液中 | |
| B. | 曲线上A点的溶液里溶质有H2SO4、Na2SO4和NaOH | |
| C. | 取曲线上M点的溶液,向其中滴入无色酚酞试液,溶液变红色 | |
| D. | 曲线上B点的溶液里溶质有两种 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4 Na2SO4 KNO3 | B. | CuSO4 H2SO4 NaCl | ||
| C. | NaOH NaCl HCl | D. | H2SO4 Na2CO3 NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| NaHCO3 | Na2CO3 | ||||
| 0.1% | 1% | 5% | 0.1% | ||
| CaCl2 | 0.1% | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 1% | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 5% | 无明显现象 | 有浑浊 | 有沉淀,有大量气泡 | 有沉淀 | |
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验1 |  | 向2支试管中分别加入少量Na2CO3和NaHCO3溶液,再分别滴加盐酸 | 2支试管中均有气泡产生 |
| 实验2 |  | 向II中加入试剂a,向I中加入少量Na2CO3或NaHCO3固体,分别加热一段时间 | Na2CO3受热时II中无明显现象 NaHCO3受热时II中出现浑浊 |
| 实验3 | 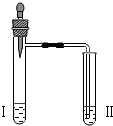 | 向II中加入试剂a,向I中加入少量5%的NaHCO3溶液,再滴加5%的CaCl2溶液 | I中出现浑浊,有气泡产生 II中出现浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com