
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物进行系列实验。
(査阅资料)碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:![]() 。
。
(进行实验)实验1:取质量比1:11的木炭粉和氧化铜混合物![]() ,进行实验。
,进行实验。
序号 | | |
装置 |
|
|
反应后物质的 颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定量的混合物,用1-2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
| 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 1:10 | 混有很少量黑色物质 | |
| 1:11 | 混有极少量黑色物质 | |
| 1:12 | 无黑色物质 | |
| 1:13 | 混有较多黑色物质 | |
(1)实验![]() 中,证明产生了
中,证明产生了![]() 的现象是______。
的现象是______。
(2)实验![]() 比
比![]() 更好的原因是______。
更好的原因是______。
(3)实验2的结论是______。
(反思与评价)
(4)实验2没有进行质量比为1:14的实验,理由是______。
(5)为检验![]() 的红色固体中是否
的红色固体中是否![]() 请你设计实验方案三
请你设计实验方案三![]() 方法、现象及结论
方法、现象及结论![]()
方法:______。可能的现象及结论______。
【答案】澄清石灰水变浑浊 使热量聚集,更好的加热氧化铜 木炭与氧化铜质量比为1:12时恰好完全反应,因此木炭与氧化铜反应的最佳质量比为1:12 木炭与氧化铜的质量比为1:13时,氧化铜已过量 取样品,加入稀硫酸 溶液由无色变成蓝色,且有红色固体剩余,样品中含有氧化亚铜
【解析】
(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以实验![]() 中,证明产生了
中,证明产生了![]() 的现象是:澄清石灰水变浑浊;
的现象是:澄清石灰水变浑浊;
(2)通过分析反应装置可知,实验![]() 比
比![]() 更好的原因是:使热量聚集,更好的加热氧化铜;
更好的原因是:使热量聚集,更好的加热氧化铜;
(3)实验2提供的数据以及实验现象可以看出,木炭与氧化铜质量比为1:12时恰好完全反应,因此木炭与氧化铜反应的最佳质量比为1:12;
(4)实验2没有进行质量比为1:14的实验,是因为当木炭与氧化铜的质量比为1:13时,氧化铜已过量;
(5)检验④的红色固体中含有![]() 的方法是:向红色固体中加入足量的稀硫酸,可以观察到溶液由无色变成蓝色,且有红色固体剩余。
的方法是:向红色固体中加入足量的稀硫酸,可以观察到溶液由无色变成蓝色,且有红色固体剩余。


科目:初中化学 来源: 题型:
【题目】发生下列情况时,所采取的对应措施正确的是![]()
![]()
A. 室内发生火灾时,打开所有门窗通风
B. 发现燃气泄漏应关闭阀门并开窗通风
C. 启用闲置的沼气池前先进行火把照明
D. 煤气泄漏时,打开电灯检查漏气管道
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国海岸线曲折,海洋资源十分丰富。
(1)如图所示,从海水中获得淡水的方法是______,你认为该技术的优点是______。
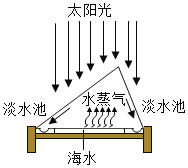
(2)从海水中提取金属镁,可按如图所示流程进行:

①写出步骤Ⅱ发生反应的化学方程式______;
②根据流程图,下列说法正确的是______(选填字母序号)。
A、步骤Ⅰ通过一步反应即可实现
B、步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C、步骤Ⅲ发生了中和反应
D、步骤Ⅴ中化学能转化为电能
(3)我国著名化学家侯德榜发明的“联合制碱法”主要工艺流程示意图如下:
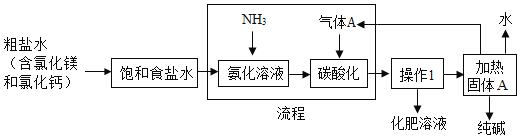
①为了除去粗盐水中可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为______。
a.稍过量的Na2CO3溶液b.适量的盐酸c.稍过量的Ba(OH)2溶液
②流程一,氨化溶液后,溶液的pH______7(选填“>”、“<”或“=”),从而有利于吸收气体A,流程一反应的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】类推是化学学习中常用的思维方法。下列类推结果正确的是![]()
![]()
A. CO、![]() 在氧气中燃烧都能生成
在氧气中燃烧都能生成![]() ,则在氧气中充分燃烧能生成
,则在氧气中充分燃烧能生成![]() 的物质一定含有碳元素
的物质一定含有碳元素
B. 单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质
C. 化学变化伴随有能量变化,所以有能量变化的一定是化学变化
D. 离子是带电荷的微粒,所以带电荷的微粒一定是离子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用下列装置制取气体,请你根据所学知识回答下列问题.
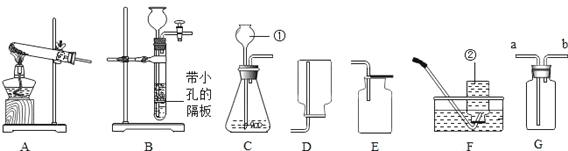
(1)写出编号所指仪器的名称:①_____;②_____.
(2)以上装置图中有一处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:(上述装置改正后,请继续回答下列问题.)_________
(3)欲制取并收集一瓶纯净的氧气并且要求能能随时控制反应进程,应选用的装置是_________(填字母)
(4)实验室选用C和E装置可以制取的气体是_____(填化学式),写出实验室制取该气体的化学方程式___________.
(5)有一名同学欲用G装置收集H2,则H2应从导管口_____通入.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有某铝铁锌合金(A1﹣Fe-Zn)样品8.3g,将其放入200g稀硫酸中,经测定恰好完全反应,蒸发结晶,称量所得固体质量为27.5g,则所用稀硫酸的溶质质量分数为( )
A. 9.8% B. 6.26% C. 22.6% D. 19.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:
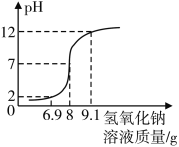
步骤一:配制溶质质量分数为10%的氢氧化钠溶液。
步骤二:向20 g待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图象如图。
(1)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质有___。(用化学式表示)
(2)请结合图,计算该稀盐酸的溶质质量分数__________。(结果精确到0.01%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】很多饮料中含有柠檬酸(C6 H8 O7)。下列关于柠檬酸的说法中正确的是![]()
![]()
A. 柠檬酸由6个碳原子、8个氢原子和7个氧原子组成
B. 柠檬酸中碳、氢、氧三种元素的质量比为6:8:7
C. 柠檬酸中碳元素的质量分数最大
D. 柠檬酸完全燃烧生成CO2、H2 O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com