
(09肇庆)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:
(NH4)2SO4+2NaOH△Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 == (NH4)2SO4 。
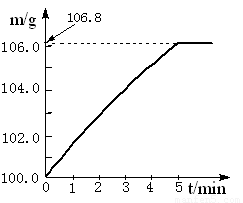
请计算:
(1)完全反应后产生氨气 g。
(2)该化肥的含氮量为 (精确到0.1%),则这种化肥属于 (填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是 。
(1)(1分)6.8g
(2)(2分)20.4% 合格
(3)解:设废硫酸中纯硫酸的质量为x 。
2NH3 + H2SO4 == (NH4)2SO4,
34 98
6.8g x ...............(1分)
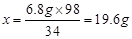
...........................................................(1分)
H2SO4%=(19.6g÷100.0g)×100%=19.6% .....................................(1分)
答:废硫酸中硫酸的质量分数为19.6%。
(4)(1分)加热反应产生的水蒸汽被废硫酸吸收,导致所测吸收液质量比只吸收氨气大。
【解析】略


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源: 题型:
(09肇庆)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:
(NH4)2SO4+2NaOH△Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 == (NH4)2SO4。
请计算:
(1)完全反应后产生氨气 g。
(2)该化肥的含氮量为 (精确到0.1%),
则这种化肥属于 (填:“合格”或“不合格”。
合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算
过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2009年全国中考化学试题分类汇编考点11 化学方程式(二) 题型:计算题
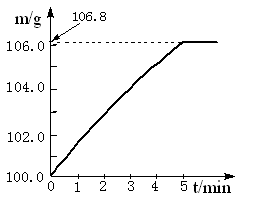
(09肇庆)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:
(NH4)2SO4+2NaOH△Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 ==(NH4)2SO4。
请计算:
(1)完全反应后产生氨气 g。
(2)该化肥的含氮量为 (精确到0.1%),
则这种化肥属于 (填:“合格”或“不合格”。
合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算
过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是 。
查看答案和解析>>
科目:初中化学 来源:2009年全国中考化学试题分类汇编考点11化学方程式(二) 题型:计算题
(09肇庆)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:
(NH4)2SO4+2NaOH△Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 == (NH4)2SO4 。
请计算:

(1)完全反应后产生氨气 g。
(2)该化肥的含氮量为 (精确到0.1%),
则这种化肥属于 (填:“合格”或“不合格”。
合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算
过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com