
·ÖĪö “Ó¶žŃõ»ÆĢ¼²»µ«ÄÜČÜÓŚĖ®£¬¶ųĒŅ»¹ÄÜøśĖ®·“Ó¦£¬Éś³ÉĢ¼Ėį£»Ģ¼Ėį²»ĪČ¶Ø£¬ÓÖ»į·Ö½ā³ÉĖ®ŗĶ¶žŃõ»ÆĢ¼Č„·ÖĪö£®
½ā“š ½ā£ŗ¶žŃõ»ÆĢ¼²»µ«ÄÜČÜÓŚĖ®£¬¶ųĒŅ»¹ÄÜøśĖ®·“Ó¦£¬Éś³ÉĢ¼Ėį£¬Ęä·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½ĪŖ£ŗ¶žŃõ»ÆĢ¼+Ė®”śĢ¼Ėį£»Ģ¼ĖįŹĒŅ»ÖÖĖį£¬ÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģ£»Ģ¼Ėį²»ĪČ¶Ø£¬ÓÖ»į·Ö½ā³ÉĖ®ŗĶ¶žŃõ»ÆĢ¼£¬Ęä·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½ĪŖ£ŗĢ¼Ėį”śĖ®+¶žŃõ»ÆĢ¼£»
¹Ź“š°øĪŖ£ŗĢ¼Ėį Ė®ŗĶ¶žŃõ»ÆĢ¼ ¶žŃõ»ÆĢ¼+Ė®”śĢ¼Ėį Ģ¼Ėį”śĖ®+¶žŃõ»ÆĢ¼£®
µćĘĄ ĢāÄæÄŃ¶Č²»“ó£¬Ö÷ŅŖæ¼²éĮĖ¶žŃõ»ÆĢ¼ŗĶĖ®µÄ·“Ó¦”¢Ģ¼ĖįµÄ²»ĪČ¶ØŠŌ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
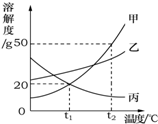
| A£® | ŅŖÅäÖĘĻąĶ¬ÖŹĮæ·ÖŹżµÄ¼×”¢±ūĮ½ÖÖĪļÖŹµÄ±„ŗĶČÜŅŗ£¬Ó¦øĆ½«ĪĀ¶ČæŲÖĘŌŚt1”ę | |
| B£® | t2”ꏱ£¬30g ¼×ĪļÖŹ¼ÓČėµ½50gĖ®ÖŠ²»¶Ļ½Į°č£¬ŠĪ³ÉµÄČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżŹĒ37.5% | |
| C£® | ŅŖ“Ó»ģÓŠÉŁĮæŅŅĪļÖŹµÄ¼×ĪļÖŹÖŠ»ńµĆ¼×£¬æÉŅŌ²ÉÓĆ½µĪĀ½į¾§µÄ·½·Ø | |
| D£® | t1”ꏱ£¬½«ČżÖÖĪļÖŹµÄ±„ŗĶČÜŅŗÉżĪĀÖĮt2”ę£¬ĖłµĆČÜŅŗÖŠČÜÖŹÖŹĮæ·ÖŹżŅŅ£¾¼×£¾±ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 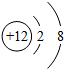 | B£® | 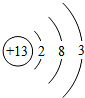 | C£® | 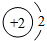 | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
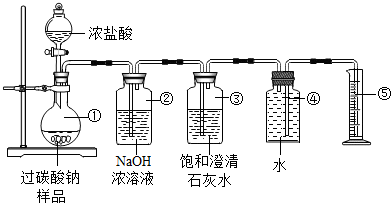
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±¬ÕØ | B£® | Īüø½ | C£® | Éż»Ŗ | D£® | Č¼ÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ӱӢӡ
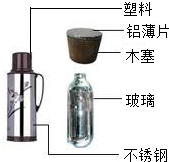
”±”¢”° ”±±ķŹ¾²»Ķ¬ŌŖĖŲµÄŌ×Ó£¬ČēĶ¼Ėł±ķŹ¾µÄĘųĢåĪļÖŹÖŠ£ŗŹōÓŚ»ģŗĻĪļµÄŹĒ£Ø””””£©
”±±ķŹ¾²»Ķ¬ŌŖĖŲµÄŌ×Ó£¬ČēĶ¼Ėł±ķŹ¾µÄĘųĢåĪļÖŹÖŠ£ŗŹōÓŚ»ģŗĻĪļµÄŹĒ£Ø””””£©| A£® |  | B£® |  | C£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé·½°ø | ²āČÜŅŗpH | µĪ¼ÓNa2CO3ČÜŅŗ | µĪ¼ÓBaCl2ČÜŅŗ |
| ŹµŃé²Ł×÷ | 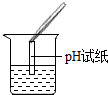 |  |  |
| ŹµŃéĻÖĻó | ŹŌÖ½±äÉ«£¬¶Ō±Č±ČÉ«æØ£¬pH£¼7 | ÓŠĘųÅŻ²śÉś | ²śÉś°×É«³Įµķ |
| ŹµŃé½įĀŪ | ČÜŅŗÖŠÓŠH2SO4 | ČÜŅŗÖŠÓŠH2SO4 | ČÜŅŗÖŠÓŠH2SO4 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com