
 水是重要的自然资源,是人类赖以生存的物质基础.
水是重要的自然资源,是人类赖以生存的物质基础.

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
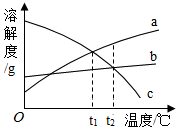
 a、b、c三种固体物质的溶解度曲线如图所示.下列说法正确的是( )
a、b、c三种固体物质的溶解度曲线如图所示.下列说法正确的是( )| A、t1℃时,a、b、c三种物质的溶解度由大到小的顺序是b>a>c |
| B、t2℃时,30 g a物质加入到50 g水中不断搅拌,所得溶液溶质质量分数为37.5% |
| C、将t1℃时c的饱和溶液升温到t2℃,变为不饱和溶液 |
| D、t2℃时,将相同质量的a、b、c三种物质的饱和溶液降温到t1℃,析出晶体最多的是a |
查看答案和解析>>
科目:初中化学 来源: 题型:
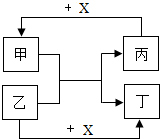 甲、乙、丙、丁、X是水、二氧化碳、盐酸、氢氧化钠、氢氧化钙、碳酸钠、碳酸钙中的一种,常温下它们的转化关系如图所示(部分反应的生成物未全部标出),下列推断正确的是( )
甲、乙、丙、丁、X是水、二氧化碳、盐酸、氢氧化钠、氢氧化钙、碳酸钠、碳酸钙中的一种,常温下它们的转化关系如图所示(部分反应的生成物未全部标出),下列推断正确的是( )| A、若X是氢氧化钠,则丁一定是水 |
| B、若X是盐酸,则丙一定是碳酸钙 |
| C、若X是二氧化碳,则乙一定是氢氧化钠 |
| D、若X是氢氧化钙,则丙一定是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用硫酸铜溶液浸泡粽子叶,包出的粽子色泽艳丽,营养丰富 |
| B、利用高温杀毒的原因是能够破坏蛋白质的生理活性 |
| C、用洗洁精清洗餐具上的油污 |
| D、尼古丁是一种剧毒兴奋剂,会使吸烟者产生依赖,所以我们要拒绝烟草 |
查看答案和解析>>
科目:初中化学 来源: 题型:
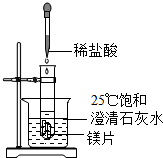 化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.
化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.查看答案和解析>>
科目:初中化学 来源: 题型:
| 成分 | SiO2 | AlO3 | Fe2O3 | CuO | SO2 |
| 质量分数/% | 50.6 | 28.9 | 8.4 | 8.6 | 3.5 |
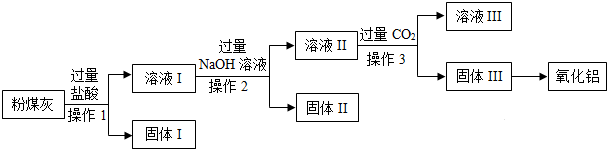
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 解释或结论 |
| (1)将清新洁净的空气通过NaOH溶液,再通过浓硫酸. | ①通过NaOH溶液的目的是除去空气中的二氧化碳;该反应的化学方程式 ②通过浓硫酸的目的是为了除去空气中的 |
| (2)将气体通过能红热的铜 | 除尽空气中氧气的化学方程式是 |
| (3)收集剩余气体,并测定其密度 | 密度为1.2572克/升 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 水是最普通、最常见的物质之一.
水是最普通、最常见的物质之一.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com