蛋壳中含有碳酸钙,兴趣小组的同学对蛋壳进行如下探究:
(1)证明蛋壳中含有碳酸根,其方法是______;
(2)用镊子取一片蛋壳在酒精灯外焰上加热,蛋壳变为白色,该过程中发生反应的化学方程式为______ CaO+CO2↑
【答案】
分析:(1)验证物质含有碳酸根,需要将之转化为二氧化碳后检验二氧化碳,所以需要用到盐酸和石灰水具体才做可以个性化.
(2)碳酸钙在高温时能够分解为氧化钙和二氧化碳,而氧化钙在水中能够生成氢氧化钙,显碱性.
(3)计算蛋壳中的碳酸钙的质量分数,指需要根据二氧化碳的生成量求算出碳酸钙的质量,进而求算其质量分数.
解答:解:(1)验证蛋壳含有碳酸根,由于不可溶,所以无法借助生成碳酸钙的现象确定,需要将之转化为二氧化碳,之后再用石灰水确定二氧化碳的存在.故答案为:将粉碎后的蛋壳中加到盛有稀盐酸的烧杯中,再将涂有澄清石灰水的玻璃片罩在烧杯上,观察石灰水是否变浑浊.变浑浊则原物质一定含有碳酸根,否则就不含.(其他方法,合理也可).
(2)碳酸钙在高温时分解为氧化钙和二氧化碳,而氧化钙遇到水能够生成碱性的氢氧化钙,而碱性的氢氧化钙能使酚酞变成红色.
故答案为:CaCO
3
CaO+CO
2↑;红;CaO+H
2O=Ca(OH)
2.
(3)设3.2g蛋壳中含有的碳酸钙的质量为x.
CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑
100 44
x 0.88g

=

x=2g.
则蛋壳中碳酸钙的质量分数为
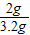
×100%=62.5%
答:蛋壳中碳酸钙的质量分数为62.5%
点评:进行计算时含有杂质的数值不能用于方程式的计算.而验证物质含有碳酸根时,原理是先转化后检验,而具体的操作多样化.

 CaO+CO2↑;红;CaO+H2O=Ca(OH)2.
CaO+CO2↑;红;CaO+H2O=Ca(OH)2. =
=
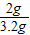 ×100%=62.5%
×100%=62.5%

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案