
【题目】溶液与人们的生产生活密切相关。
(1)将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是_____(填字母)。
A.高锰酸钾 B.汽油 C.面粉 D.白糖
(2)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度没有明显变化的 是_____ (填字母)。
A.烧碱 B.硝酸铵 C.氯化钠 D.浓硫酸
(3)下图 1 为甲、乙两种固体物质的溶解度曲线。
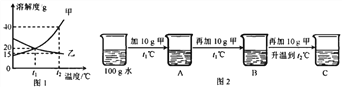
①溶解度随温度升高而增大的物质是_____(填 “甲”或“乙”)。
②某同学按图 2 所示进行实验,得到相应温度下的 A、B、C 溶液,在 A、B、C 三种 溶液中属于饱和溶液的是________(填字母)。向溶液 C 中再加入 25g 甲,充分搅拌, 恢复到 t2℃时,所得溶液中溶质的质量分数为_______________(结果精确到 0.1%)。
③将 t2℃时的甲、乙两种物质的饱和溶液降温至 t1℃,所得溶液中溶质的质量分数 甲_____乙(填“<”、“=”或“>”)。
【答案】D C 甲 B 28.6% >
【解析】
(1)A.高锰酸钾溶于水是紫色溶液,不符合题意;B.汽油难溶于水,不能形成溶液,不符合题意;C.面粉难溶于水,不能形成溶液,不符合题意;D.白糖溶于水是无色溶液,符合题意。故选D。(2)A.烧碱溶于水放出大量的热,温度升高,不符合题意;B.硝酸铵溶于水吸收大量的热,温度降低,不符合题意;C.氯化钠溶于水温度变化不明显,符合题意;D.浓硫酸溶于水放出大量的热,温度升高,不符合题意。故选C。(3)①由溶解度曲线看出,甲的溶解度随温度升高而增大。②t1℃时,甲的溶解度是20g,则在t1℃时,100g水中最多能溶解20g甲;t2℃时,甲的溶解度是40g,则在t2℃时,100g水中最多能溶解40g甲,所以B是饱和溶液。C中加入甲的质量是10g+10g+10g+25g=55g,溶液C中最多溶解40g甲,所以C溶液中溶质的质量分数为:![]() ×100%= 28.6%。③t2℃时,乙的饱和溶液降温时,溶解度增大,溶质质量分数不变,甲的溶解度减少,溶质质量分数减小,因为t1℃甲的溶解度大于t2℃时乙的溶解度,所以t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲>乙。
×100%= 28.6%。③t2℃时,乙的饱和溶液降温时,溶解度增大,溶质质量分数不变,甲的溶解度减少,溶质质量分数减小,因为t1℃甲的溶解度大于t2℃时乙的溶解度,所以t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲>乙。


科目:初中化学 来源: 题型:
【题目】氧气是我们身边无法离开的物质。某兴趣小组对氧气的研究如下:
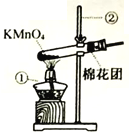
I.氧气的制备:
(1)写出上图中有标号仪器的名称:①___________,②__________。
(2)写出用KMnO4制取O2的化学反应方程式__________________。该装置中棉花团的作用是_________________,图中装置一处明显的错误是______________。
II.氧气的收集:
[实验1]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
[实验2]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
[实验3]用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1 | 实验2 | 实验3 | |||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 | ||||||
数据
(3)由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是_______________。
(4)不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_______。
Ⅲ.铁丝在氧气中燃烧
(5)铁丝在纯净氧气中燃烧的化学反应方程式为________________________。
(6)铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是_____________(填化学式)。将燃烧后的黑色固体粉碎后,滴加稀盐酸,若产生气泡,则原因是________________(用化学反应方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列所示的四个图像, 能正确反映对应变化关系的是
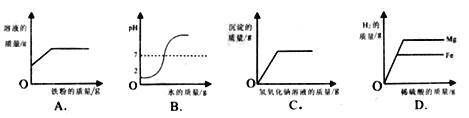
A. 向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B. 向pH=2的盐酸中加水稀释
C. 向一定量的含有盐酸的氯化铜溶液中滴加氢氧化钠溶液
D. 等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在通常状况下,硫是一种黄色粉末,下图是硫元素的某种粒子的结构示意图:
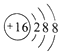
(1)硫原子的核内质子数为_________。
(2)图中所示粒子的符号为_________。
(3)硫在氧气中燃烧,发出蓝紫色火焰,该反应的化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海螵蛸是一味中药,其主要成分是碳酸钙,某同学利用如图装置测定其中碳酸钙的含量。
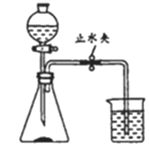
①在锥形瓶中加入质量为m的海螵蛸粉末,向分液漏斗中加入稀盐酸。在烧杯中加人足量氢氧化钠溶液,并称量烧杯及氢氧化钠溶液总质量m1
②先打开止水夹,再打开分液漏斗活塞,滴加盐酸并及时关闭活塞。完全反应后,再次称量烧杯及其中液体的总质量m2.
③利用m2与m1的差值,即反应生成的二氧化碳质量,再计算海螵蛸中碳酸钙的含量。
(1)海螵蛸具有治疗胃酸过多、能为骨质发育提供重要元素的功效,其原因是___________。
(2)实验前要检查装置的气密性,方法是:用止水夹夹住橡胶管,往分液漏斗中加入适量水。打开分液漏斗的活塞.观察到_______,说明装置气密性 良好。
(3)下列情况会导致海螵蛸中碳酸钙质量分数测量值偏小的是______(可多选)。
A.海螵蛸中滴加盐酸过量
B,锥形瓶内部分水蒸气随二氧化碳逸出
C.反应结束后,锥形瓶内有二氧化碳残留
D.反应速度过快,大量气泡从氢氧化钠溶液中溢出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料广泛应用于生产生活中。
(1)常温下大多数金属都是固体,但体温计中的金属却是液体,该金属是________。
(2)铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物的化学式为________。
(3)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是___(写化学式)。
(4)铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等。
①写出赤铁矿石中的主要成分与一氧化碳反应的化学方程式________。
②冶炼2900t含四氧化三铁80%的磁铁矿石,理论上能得到含杂质2%的生铁的质量是________ t(结果精确到0.1)。
(5)含有锌粉6.5g、铁粉5.6g、铜粉3.2g、铝粉l.8g的混合物与一定质量的稀硫酸充分反应,反应停止后,有6g固体剩余。则生成氢气的质量为________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】X是常见的碳酸盐,可发生如图所示的变化,部分生成物省略。根据下图回答问题。
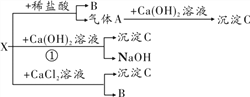
(1)C的化学式是____________________________。
(2)写出图中①反应的化学方程式:______________,该反应基本类型是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“下图”是部分元素的离子结构示意图和元素周期表的一部分。请回答:
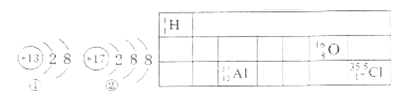
(1)图①、②中属于阴离子的是___(填序号),该元素的质子数为_____;13号元素原子的最外层电子数为_____。
(2)由表中原子序数为1、8、13的元素组成物质的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格。
将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
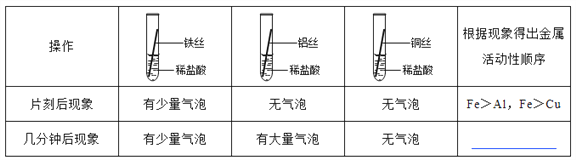
__________________
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是__________________________,
铁与盐酸反应的方程式是_________________________________________________。
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、 打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出金属活动性顺序 |
现象 | 无明显现象 | ______________________ | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式______________________________________________。
【拓展迁移】若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com