
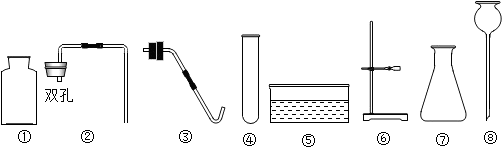
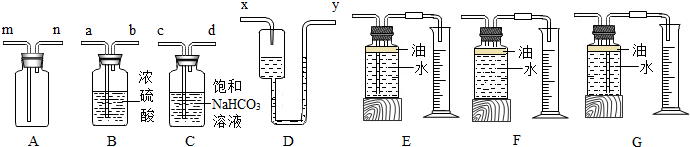
·ÖĪö £Ø1£©Źģ¼Ē³£ÓĆŅĒĘ÷µÄĆū³Ę£»
£Ø2£©øł¾ŻŹµŃéŹŅÖŠÖĘČ”¶žŃõ»ÆĢ¼µÄŅ©Ę·×“Ģ¬”¢·“Ó¦Ģõ¼ž”¢·“Ó¦ŌĄķĄ“·ÖĪö£»
£Ø3£©øł¾Ż¶žŃõ»ÆĢ¼µÄŠŌÖŹ”¢ĘųĢå³żŌÓµÄŌŌņŗĶĖ³ŠņĄ“·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©¢ŁŹĒ¼ÆĘųĘ棬¢ąŹĒ³¤¾±Ā©¶·£»¹ŹĢī£ŗ¼ÆĘųĘ棻³¤¾±Ā©¶·£»
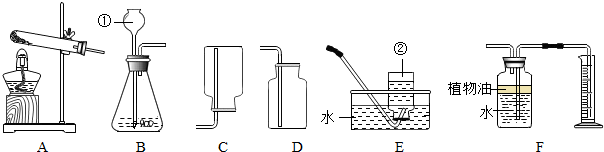
£Ø2£©ŹµŃéŹŅÖŠÖĘČ”¶žŃõ»ÆĢ¼ŠčŅŖÓƵ½æéד¹ĢĢåµÄ“óĄķŹÆ»ņŹÆ»ŅŹÆ£¬ÓėŅŗĢ¬µÄĻ”ŃĪĖįŌŚ³£ĪĀĻĀ·“Ó¦Ą“ÖĘČ”£¬ŅŖÖĘČ”½Ļ¶ąµÄĘųĢåӦєŌń׶ŠĪĘæ¶ų²»ÄÜŃ”ŌńŹŌ¹Ü£¬¶žÕß·“Ӧɜ³ÉĀČ»ÆøĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£»¹ŹĢī£ŗ¢Ś¢ß¢ą£»CaCO3+2HClØTCaCl2+H2O+CO2”ü£»
£Ø3£©¶žŃõ»ÆĢ¼µÄĆܶȱČæÕĘų“ó£¬ĖłŅŌÓĆ×°ÖĆAĄ“ŹÕ¼ÆŹ±£¬ĘųĢå“Ó³¤¹Ü½ųČė£»ÖĘČ”µÄ¶žŃõ»ÆĢ¼ÖŠ»ģÓŠÉŁĮæµÄĀČ»ÆĒāĘųĢåŗĶĖ®ÕōĘų£¬Ó¦øĆÓĆĢ¼ĖįĒāÄĘČÜŅŗĻČ³żČ„ĀČ»ÆĒāĘųĢ壬ŌŁÓĆÅØĮņĖįĄ“½ųŠŠøÉŌļ£¬ĘųĢå½ų³öĖ³ŠņĪŖ£ŗ³¤½ų¶Ģ³ö£»øĆĶ¼ŹĒŅ½ÓĆŹäŅŗ¹Ū²ģµĪŅ¹æģĀżµÄµĪŗų£¬ČōÓĆĖü×÷Ī¢ŠĶĻ“Ęų×°ÖĆ£¬ŌņĘųĢåÓ¦“Óy½ųČė£¬ĘäÖŠĖł×°Ļ“ĘųµÄŅŗĢå²»ÄÜ×°ĀśµÄŌŅņŹĒŅŗĢå²»»į±»Ń¹Ķłx“¦Į÷³ö£®ŅŖ²āĮæ²śÉśCO2Ģå»ż£¬ŅŖ“Ó¶Ģ¹Ü½ųĘų£¬³¤¹Ü³öĖ®£¬øüĄūÓŚĖ®µÄÅųö£¬“Ó¶ų²āĮæCO2Ģå»ż£»
¹Ź“š°øĪŖ£ŗm£»c£»d£»a£»b£»y£»G£®
µćĘĄ ±¾Ģāæ¼²éĮĖѧɜ¶Ō×°ÖĆєȔ”¢ŅĒĘ÷Ź¹ÓĆ”¢·“Ó¦ŌĄķ”¢ĘųĢå²āĮæµČÖŖŹ¶µÄÕĘĪÕŗĶÓ¦ÓĆ£¬ÕĘĪÕĖłŃ§ÖŖŹ¶²¢ÄܽįŗĻĢāŅā·ÖĪö½ā“šŹĒ½ā¾öĪŹĢāµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ·“Ó¦Ē°ŗóŌ×ÓÖÖĄą”¢ŹżÄæ¾ł²»±ä | |
| B£® | øĆ·“Ó¦ÖŠ£¬·“Ó¦ĪļµÄ·Ö×ÓŹżÄæ±ČŹĒ1£ŗ2 | |
| C£® | øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCH4+2O2 $\frac{\underline{\;µćČ¼\;}}{\;}$ CO2+2H2O | |
| D£® | øĆ·“Ó¦ŹĒ»ÆŗĻ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| Ń”””Ļī | ÄæµÄ | ĖłÓĆŹŌ¼Į»ņ·½·Ø |
| A | ·ÖĄėCaCl2ŗĶCaCO3 | ×ćĮæµÄĻ”ŃĪĖį”¢Õō·¢ |
| B | ¼ų±šÓ²Ė®ŗĶČķĖ® | Ć÷·Æ |
| C | ¼ģŃé¼ÆĘųĘæÖŠO2ŹĒ·ńŹÕ¼ÆĀś | ½«Č¼×ŵÄľĢõ·ÅŌŚ¼ÆĘųĘææŚ |
| D | ³żČ„CuÖŠÉŁĮæC | ×ĘÉÕ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
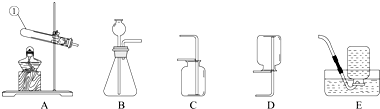
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
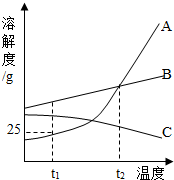 ČēĶ¼ŹĒA”¢B”¢CČżÖÖ¹ĢĢåĪļÖŹŌŚĖ®ÖŠµÄČܽā¶ČĒśĻߣ¬¾ŻĶ¼»Ų“š£ŗ
ČēĶ¼ŹĒA”¢B”¢CČżÖÖ¹ĢĢåĪļÖŹŌŚĖ®ÖŠµÄČܽā¶ČĒśĻߣ¬¾ŻĶ¼»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉĢ¼”¢ĒāĮ½ÖÖŌŖĖŲ×é³É | B£® | Ņ»øö·Ö×Óŗ¬ÓŠ10øöĒāŌ×Ó | ||
| C£® | ŹōÓŚÓŠ»śĪļ | D£® | Ģ¼”¢ĒāŌŖĖŲµÄÖŹĮæ±ČŹĒ2£ŗ5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĘĻĢŃĢĒ£ØC6H12O6£©ŹĒÉśĆü»ī¶ÆÖŠ²»æÉȱɣµÄĪļÖŹ£¬ČēĶ¼ŹĒ²”ČĖŹäŅŗÓƵÄĘĻĢŃ
ĘĻĢŃĢĒ£ØC6H12O6£©ŹĒÉśĆü»ī¶ÆÖŠ²»æÉȱɣµÄĪļÖŹ£¬ČēĶ¼ŹĒ²”ČĖŹäŅŗÓƵÄĘĻĢŃ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com