
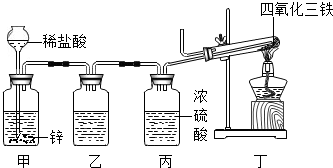
 “引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃,如图所示是用新制的四氧化三铁与纯净、干燥的氢气制备“引火铁”的装置,请回答:
“引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃,如图所示是用新制的四氧化三铁与纯净、干燥的氢气制备“引火铁”的装置,请回答:分析 (1)根据用锌和稀盐酸制取的氢气中含有氯化氢气体和水,浓硫酸有吸水性,氯化氢需要用碱液吸收进行分析;
(2)根据洗气时应该是长进短出进行分析;
(3)根据氢气的验纯方法来解答;
(4)A、根据燃烧一般都是放热反应进行分析;
B、根据氧化反应的定义进行分析;
C、根据可燃物燃烧的条件进行分析;
D、根据普通铁粉不易燃烧,而“引火铁”易自燃进行分析.
解答 解:(1)用锌和稀盐酸制取的氢气中含有氯化氢气体和水,浓硫酸有吸水性,氯化氢需要用碱液吸收,所以广口瓶乙中盛放的物质是氢氧化钠溶液;
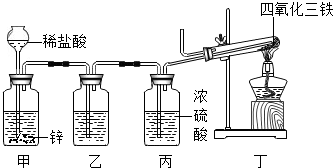
(2)洗气时应该是长进短出,所以导管在广口瓶乙中的插入情况是
(3)从导气管末端收集一小试管气体,点燃,不发出尖锐爆鸣声,说明空气已经排完;
(4)A、燃烧一般都是放热反应,所以“引火铁”的自燃是放热反应,故A错误;
B、有氧参与的反应就是氧化反应,所以“引火铁”的自燃是氧化反应,故B正确;
C、“引火铁”的自燃需要达到它的着火点,故C正确;
D、普通铁粉不易燃烧,而“引火铁”易自燃,故D正确.
故选:A.
故答案为:(1)氢氧化钠溶液;
(2)
(3)用试管在丁的出口导管处收集气体,检验氢气的纯度;
(4)A.
点评 在解此类题时,首先分析题中考查的问题,.然后结合学过的知识和题中的提示进行解答.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 灭火方法--实验桌上少量酒精着火,用湿抹布盖灭 | |
| B. | 食品安全--亚硝酸钠对人体有害,不能食用 | |
| C. | 能源与环境--煤、石油、天然气等化石燃料燃烧后的产物对环境无影响 | |
| D. | 实验安全-稀释浓硫酸时要将浓硫酸沿烧杯壁慢慢注入水中并用玻璃棒不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
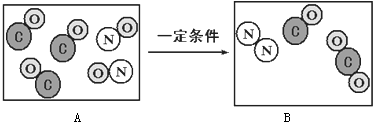
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Zn | B. | Cu | C. | Zn、Cu | D. | Cu、Mg、Zn |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
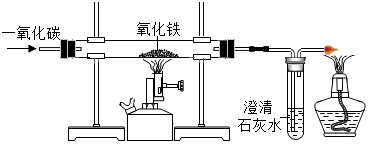
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com