
我们已经学过实验室制取气 体的一般思路和方法,请利用下列装置回答相关问题.
体的一般思路和方法,请利用下列装置回答相关问题.
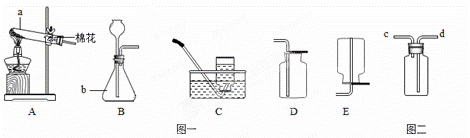
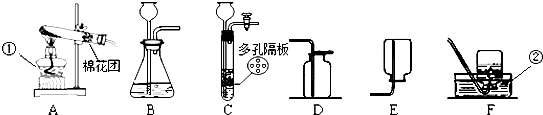
(1) 写出图一中a和b的仪器名称:a b ;
(2) 选择图一中的装置制取和收集二氧化碳气体,那么应选择的装置是 和 ;
在实验 室中制取二氧化碳气体的常用药品:液体是 ,固体是 。
室中制取二氧化碳气体的常用药品:液体是 ,固体是 。
(3) 若要用图二装置收集二氧化碳气体,则气体应从 (填c或d)端通.理由是 .
(4) 用制取的二氧化碳进行如下有关性质实验:
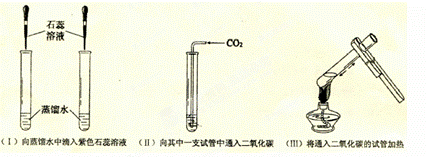
①实验(II)中溶液变 色;
②实验(III)中加热之后,溶液又变为 色,解释出现此现象的原因 。
(5) 实验室用高锰酸钾制取氧气的化学反应方程式(或化学式表达式)
 若要用排水法收集一瓶较纯净的氧气,开始收集氧气的最佳时机是 。
若要用排水法收集一瓶较纯净的氧气,开始收集氧气的最佳时机是 。
(6)同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的O2大于理论产量。针对这一现象,同学们进行了如下探究:
[提出猜想]猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的 K2MnO4和MnO2分解都放出O2。
K2MnO4和MnO2分解都放出O2。
[实验验证]同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想 错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是 。
[拓展延伸]实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快。
请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么? 。
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:初中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
. |
| ||
. |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 | 制取气体的药品 | 制取气体的反应条件 | 气体的物理性质 |
| 氯气 | MnO2固体和浓盐酸 | 需要加热 | 能溶于水,密度比空气大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com