解:(1)铁质炒菜锅是利用铁的导热性,铜制导线是利用铜的导电性,铝制易拉罐是利用铝的延展性,黄金饰品是利用金的金属光泽和延展性;
(2)铁生锈的条件是铁与氧气和水共同接触;工业炼铁的反应物是一氧化碳和氧化铁写在等号的左边,生成物是铁和二氧化碳写在等号的右边,反应条件是高温写在等号的上边,用得失氧进行配平即可,所以方程式是:3CO+Fe
2O
3
2Fe+3CO
2;
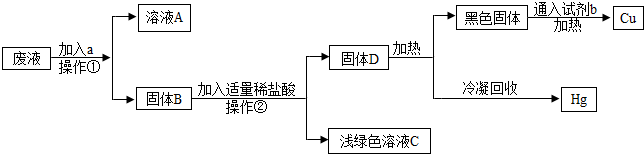
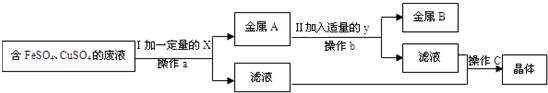
(3)Ⅰ.不溶于液体的固体和液体分离的方法是过滤;
Ⅱ.由于C溶液是浅绿色,所以含有亚铁离子,所以前面加入的金属是铁,为了将Hg(NO
3)
2、Cu(NO
3)
2中的铜和汞全部置换出来,必须加入过量的铁,所以固体B中含有被置换出来的全部的汞和铜,还有过量的铁.
故答案为:(1)A;(2)O
2、H
20或氧气、水(潮湿空气);3CO+Fe
2O
3
2Fe+3CO
2;(3)过滤;Fe或铁;Fe Cu Hg.
分析:(1)根据物质的性质决定物质的用途考虑;(2)根据铁生锈的条件和方程式的写法考虑;(3)Ⅰ根据混合物的分离方法考虑;Ⅱ根据C溶液是浅绿色说明含有亚铁离子,所以前面加入的是铁,为了反应完全要加入过量的铁再进一步进行分析即可.
点评:解答本题关键是要知道物质的性质决定物质的用途,物质的用途反映物质的性质,熟悉铁生锈的条件和方程式书写的注意事项,熟悉金属活动性顺序的应用,加强学生对知识的灵活应用.



 2Fe+3CO2;
2Fe+3CO2; 2Fe+3CO2;(3)过滤;Fe或铁;Fe Cu Hg.
2Fe+3CO2;(3)过滤;Fe或铁;Fe Cu Hg.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案