
用
FeCl2溶液、CuSO4溶液、Fe、Mg四种物质来验证Fe、Cu、Mg三种金属的活动性顺序,必须进行的两个反应是(用化学方程式表示):(1)____________________;
(2)____________________.
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:
| A、稀盐酸除铁锈2HCl+FeO=FeCl2+H20 | B、钟乳石的形成Ca(HC03)2=CaC03↓+H20+CO2↑ | C、实验室用过氧化氢溶液制氧气2H2O2=2H2O+02↑ | D、镁条在氧气中燃烧2Mg+02=MgO |
查看答案和解析>>
科目:初中化学 来源: 题型:
18、下列知识整理的内容完全正确的一组是
|
查看答案和解析>>
科目:初中化学 来源: 题型:
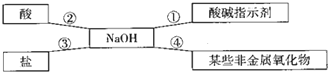 某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
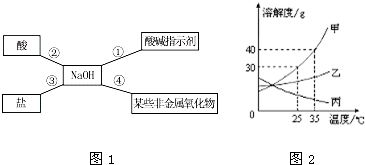
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com