
向10 g HCl、CaCl2的混合溶液中逐滴滴加溶质质量分数为10%的Na2CO3溶液直至溶液呈碱性,其中溶液的PH变化如图所示.下列有关说法正确的是
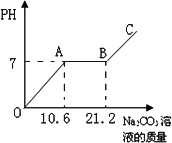
A.AB段(除端点)溶液中含有3种溶质
B.原混合溶液中HCl的溶质质量分数为7.3%
C.生成2 g的CaCO3
D.溶液中水分子的数目不变
科目:初中化学 来源:化学教研室 题型:058
(1)怎样立即确定它是不是浓盐酸?有人猜测是,有人记得好像不是,大家各抒己见.你认为,应该用下述中的________方法(填选项编号)立即确信.
A.讨论 B.调查 C.实验 D.上网
具体的做法是__________________________.
(2)粗略测定该盐酸每毫升溶液中含溶质HCl的质量.同学们依据酸和碱中和反应的原理,设计了一种可行的实验方案,其操作步骤如下:
第1步,在小烧杯中加入10 g 5%的NaOH溶液;
第2步,向上述烧杯中滴入2滴酚酞试液;
第3步,向10 mL的量筒里注入该盐酸至一定刻度;
第4步,用胶头滴管吸取量筒中的盐酸,逐滴滴入上述烧杯中……一直滴到溶液由红色刚刚变成无色为止;
第5步,记录实验数据;
第6步,计算,确定每毫升盐酸中含溶质HCl的质量.
请根据以上实验过程,回答下列问题:
①本实验为什么要用指示剂(酚酞)?____________________________
②第3步中向量筒注入盐酸,量筒中液面的位置如下图所示,A与B、B与C刻度间均相差1 mL,如果刻度A为8,量筒中盐酸的体积是________mL.

③第4步要用到玻璃棒,它是作________用,目的是____________.停止滴入盐酸后,胶头滴管中残留的盐酸应__________.
④第5步要记录的实验数据是____________________.
(3)测定每毫升该盐酸中含溶质HCl的质量,原理和方法还有多种,为此大家继续进行探究.有人提出用KOH等碱类试剂替代上述NaOH与盐酸进行中和反应,测定耗去盐酸的体积,通过计算确定盐酸中HCl的含量,这和上述实验属同一种方法.
你能写出三种其他可行的方法吗?若能,请写在下面(用文字简述所依据的原理和要测定的数据,不需要写出化学方程式):
方法一:___________________________________________________________________.
方法二:___________________________________________________________________.
方法三:___________________________________________________________________.
(4)请你在上述三种方法中,选一种,并写出按此法实验所需要的玻璃仪器.
我选的是方法______,所需要的玻璃仪器是_____________________________________.
查看答案和解析>>
科目:初中化学 来源:广西柳州市2012届九年级第一次教学质量检测化学试题 题型:013
向含CuCl2和HCl的100 g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图[仅考虑沉淀为Cu(OH)2].则下列说法不正确的是
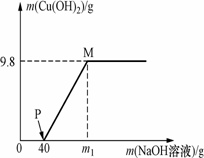
A.整个反应过程中,氯离子个数不变
B.M点溶液中的溶质只有一种
C.M点溶液比P点溶液中氯化钠的质量分数大
D.沉淀完全时,m1的数值为80
查看答案和解析>>
科目:初中化学 来源:山东省济南市2006年高中阶段学校招生考试化学部分 题型:038
在一烧杯中盛有100 g BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示:
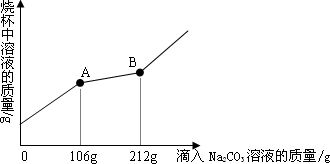
请根据题意回答问题:
(1)在实验过程中,有气体放出,还可以看到的明显实验现象是________.
(2)在实验过程中放出气体的总质量为________g.
(3)当滴入Na2CO3溶液至图中B点时,通过计算求此所得不饱和溶液中溶质质量分数是多少?(计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源:2012年江苏省南通如东中考模拟化学试卷(带解析) 题型:探究题
(10分)某研究性学习小组设计并进行了如下实验。
(1)甲组同学用右图装置制取干燥纯净的二氧化碳气体。请回答下列问题:
①仪器X的名称是 。实验前,关闭活塞,向X中加入水使X中液面高于试管中的液面,一段时间后液面保持不变说明 。
②为除去CO2中混有的HCl气体,B装置中盛放饱和NaHCO3溶液,写出该反应的化学方程式 。
③要得到干燥的CO2,C装置应盛放 (填试剂名称)。
④请说明装置B、C中试剂不能交换的原因: 。
(2)乙组同学围绕CO还原CuO产生的红色固体是否一定是Cu进行探究:
【查阅资料】 ①Cu2O粉末呈红色。在酸性溶液中:Cu2O+H2SO4=Cu+ CuSO4+H2O
②在空气中高温灼烧时:Cu2O稳定,而CuO将分解生成Cu2O和O2
【提出猜想】猜想Ⅰ:红色固体是Cu; 猜想Ⅱ:红色固体是Cu2O;
猜想Ⅲ:红色固体是 。
【实验探究】步骤Ⅰ:取一定质量的红色固体a g ,在空气中高温灼烧,直到质量不再发生改变,称量所得固体质量为b g 。
步骤Ⅱ:数据分析
①若a =" b," 则猜想 成立;
②若b>a, 则说明红色固体中一定含有 物质;
步骤Ⅲ:另取少量红色固体投入稀硫酸中,充分反应后溶液呈蓝色。根据此现象,该红色固体中含有 。写出由Cu生成Cu2O的化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com