

分析 (1)金属越活泼,人类大规模开发利用的时间越晚;
(2)铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜;
(3)根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断;
(4)铝土矿中含有氧化铝和杂质,要生产相同质量的铝,所需铝土矿的质量应大于氧化铝质量.
解答 解:(1)金属的活动性越强,即金属越活泼,越难冶炼,人类大规模开发利用的时间越晚,因此金属大规模开发利用的先后顺序与地壳中金属元素的含量无关.
故填:B.
(2)铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.
故填:Fe+CuSO4=FeSO4+Cu.
(3)设生成铝的质量为x,
2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑,
204 108
51t x
$\frac{204}{51t}$=$\frac{108}{x}$,
x=27t,
答:最多可生产27t铝.
(4)铝土矿中含有氧化铝和杂质,要生产相同质量的铝,所需铝土矿的质量应大于氧化铝质量.
故填:大于.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 名师点拨卷系列答案
名师点拨卷系列答案科目:初中化学 来源: 题型:解答题
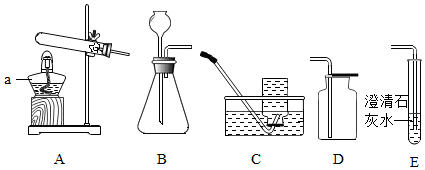 根据如图所示的装置回答有关问题
根据如图所示的装置回答有关问题查看答案和解析>>
科目:初中化学 来源: 题型:解答题
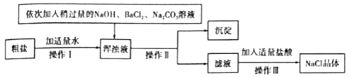
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ③④⑤①② | B. | ④⑤③①② | C. | ③①⑤②④ | D. | ⑤④①③② |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KOH Na2CO3 HCl | B. | KNO3 NaCl NaOH | ||
| C. | KNO3 NaOH FeCl3 | D. | AgNO3 BaCl2 HNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
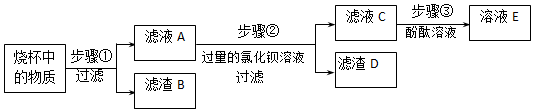
| 实验操作 | 现象 | 结论 |
| 步骤③中,加入酚酞溶液 | 若溶液E为无色 | 原白色粉末的组成是硫酸钡、碳酸钾; |
| 若溶液E为红色 | 滤液A中一定含有的溶质是氢氧化钾, 原白色粉末的可能组成分别是碳酸钾和氢氧化钡或硫酸钡、碳酸钾和氢氧化钡. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com