
某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其他杂质不与盐酸反应)。试计算:
(1)用10克30%的浓盐酸配制成2%的稀盐酸,需加水多少克?
(2)取20克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸7.3克,求废水中氢氧化钾的质量分数。
第(1)题,用10克30%的浓盐酸配制成2%的稀盐酸需要向溶液中加入水,加水的过程中,溶质的质量是不变的。可根据这一点来计算。第(2)题7.3克盐酸中氯化氢的质量为7.3 g×2%,根据化学方程式可以求出反应物氢氧化钾的质量。然后用氢氧化钾的质量比上20 g废水便得废水中氢氧化钾的质量分数。
答案:解:(1)配制2%的稀盐酸的质量为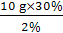 =150 g
=150 g
加入水的质量为150 g-10 g=140 g
(2)设参加反应的氢氧化钾的质量为x
HCl + KOH====KCl+H2O
36.5 56
7.3 g×2% x
36.5∶56=(7.3g×2%)∶x x=0.224 g
废水中氢氧化钾的质量分数为
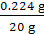 ×100%=1.12%
×100%=1.12%
答:略


科目:初中化学 来源: 题型:
在学习碱的性质时,为了验证溶液中的氢氧化钠能与二氧化碳反应,老师做了下面两个实验。
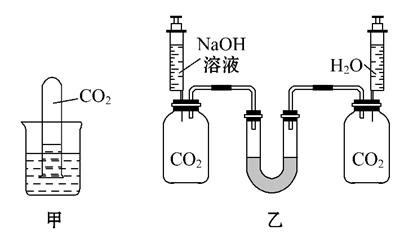
实验一:如图甲,将一支充满二氧化碳的试管倒扣在盛有氢氧化钠溶液的烧杯中,观察试管中的液面变化情况。
实验二:如图乙,向两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠溶液和蒸馏水,振荡后放在水平的桌面上,观察U形管(装有红墨水)两端液面
的 变化情况。请问:
变化情况。请问:
(1)实验二中若观察到U形管左端的液面 (填“升高”或“降低”),则证明溶液中的氢氧化钠能与二氧化碳反应。
(2)与实验一相比,同学们认为实验二更合理,因为它能排除 对实验的干扰。
查看答案和解析>>
科目:初中化学 来源: 题型:
在生活、生产和科学研究中,常用pH试纸测定溶液的pH。以下测定操作正确的是 ( )
A.将被测液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较
B.将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较
C.先用少量水湿润试纸,后滴上被测液,显色后,与标准比色卡比较
D.先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较
查看答案和解析>>
科目:初中化学 来源: 题型:
请根据下表回答有关问题,除(2)题外其余各小题均用序号填空。
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
(1)表中的物质属于氧化物的 是 ;属于碱的是 ;属于盐的是 。
是 ;属于碱的是 ;属于盐的是 。
(2)利用表中的物质作为反应物,写出符合下列要求的化学方程式。
①有氧气生成的分解反应 ___________;
②有氢氧化钠生成的复分解反应 _________。
(3)若要测定纯碱溶液的酸碱度,可选用下列选项中的 。
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
(4)槟榔芋皮上含有一种碱性的物质——皂角素,皮肤沾上它会奇痒难忍。你认为可选用下列 来涂抹止痒。
①食醋(含醋酸) ②熟石灰 ③纯碱
查看答案和解析>>
科目:初中化学 来源: 题型:
氢是新型清洁能源,但储存运输难。研究发现,镧和镍的一种合金是储氢材料,可被用于大型电池,尤其是电动车辆等。下列关于57号镧的说法不正确的是
A.该元素原子的质子数为57 B.该元素原子的核电荷数数为57
C.该元素原子的核外电子数为57 D.该元素为非金属元素
查看答案和解析>>
科目:初中化学 来源: 题型:
下列突发事故的处理措施正确的是
A.有人不慎跌入含有大量二氧化碳的深洞中,应立即下洞救人
 B.厨房中的煤气大量泄漏时,应立即关闭气阀,不能打开抽油烟机排气
B.厨房中的煤气大量泄漏时,应立即关闭气阀,不能打开抽油烟机排气
C.家中电器着火,应马上用水浇灭
D.图书档案起火,用泡沫灭火剂灭火
查看答案和解析>>
科目:初中化学 来源: 题型:
酸奶中含有的乳酸对健康是有益的。下列关于乳酸的叙述错误的是( )
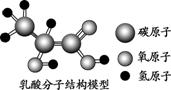
A.乳酸属于有机化合物
B.乳酸分子中碳、氢、氧的原子个数比为1∶1∶2
C.乳酸中氧元素的质量分数最大
D.乳酸由碳、氢、氧三种元素组成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com