

| A. | 一般水果有酸味,是因为水果中含有各种果酸 | |
| B. | 食醋有酸味,可大量食用 | |
| C. | 很多酸有毒不能食用 | |
| D. | “酸”一词从有酸味而来 |
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
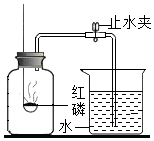 某同学用如图进行空气中氧气含量的测定的实验,回答下列问题:
某同学用如图进行空气中氧气含量的测定的实验,回答下列问题:| 实验方法和步骤 | 现象和结论 | |
| 物理方法 | 分别闻液体的气味 | 有特殊香味的是酒精,无味的是石灰水 |
| 化学方法 | 分别取适量待测液,点燃 | 能够被点燃的是酒精,不能被点燃的是石灰水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 置换反应 | C. | 分解反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我国是电池生产和消费大国,目前年产量达140亿枚,占世界产量$\frac{1}{3}$.年消费量达70-80亿只,但回收率却不足2%.关爱身边环境、参与废旧电池的分类回收利用是我们每一个人的责任和义务.如图是某锌锰干电池的剖面图片.
我国是电池生产和消费大国,目前年产量达140亿枚,占世界产量$\frac{1}{3}$.年消费量达70-80亿只,但回收率却不足2%.关爱身边环境、参与废旧电池的分类回收利用是我们每一个人的责任和义务.如图是某锌锰干电池的剖面图片.| 实验步骤 | 实验现象 | 实验结论 |
| ①剥开干电池,取出碳棒周围的黑色粉末 | / | / |
| ②为分离出氯化铵先将黑色固体溶于水,再过滤. | 得到黑色固体和无色溶液. | 黑色粉末为MnO2、C. |
| ③将黑色粉末加热灼烧. | / | 得到纯净的二氧化锰固体. |
| 取②步中得到的少量无色溶液于试管,加NaOH,加热,在试管口放湿润的红色石蕊试纸. | 有强烈刺激性气味气体产生,湿润的红色石蕊试纸变蓝色 | 溶液中含有氯化铵. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 编号 | ① | ② | ③ | ④ |
| 常用物质 | 食醋 | 白酒 | 石灰水 | 纯碱 |
| 主要成分 | CH3COOH | C2H5OH | Ca(OH)2 | Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
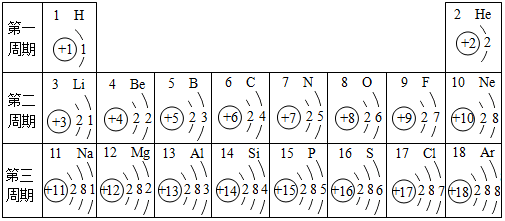
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com