
现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2 = CaCO3↓+2NaCl)。反应时CaCl2溶液与沉淀的质量关系如图所示。请解决以下问题:
(1)计算样品中NaOH的质量;
(2)计算所加CaCl2溶液的溶质质量分数;
(3)恰好完全反应时烧杯中溶液的pH______7(选填“>”、“<”或“=”)
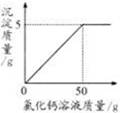
(1)解:设样品中碳酸钠的质量为x,加入的氯化钙溶液中的溶质质量为y
Na2C03+CaCl2=CaC03↓ +2NaCl
106 111 100
x Y 5 g
106/100=x/5g
x=5.3 g………………………………1分
该样品中NaOH的质量为l0 g-5.3 g=4.7 g ……………………1分
(2)111/y=100/5g
y= 5.55 g ……………………………………………………… l分
所加CaCl2溶液的溶质质量分数=5.55g/50g×l00%=111% 1分
答:样品中NaOH的质量为4.7 g,所加CaCl2溶液的溶质质量分数为ll.1%
设、答完整1分
(3)> …………………………………………………………1分


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
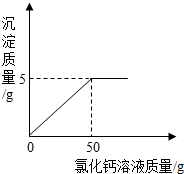 现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 现称取变质的氢氧化钠样品l0g,配制成溶液,再向其中逐滴加入CaCl2溶液.CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
现称取变质的氢氧化钠样品l0g,配制成溶液,再向其中逐滴加入CaCl2溶液.CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com