
【题目】太阳能汽车利用太阳能来驱动,真正实现了零排放,有效地减少了对环境的污染,其产业的发展日益蓬勃。从某种意义上讲,太阳能汽车也是电动汽车的—种,所不同的是电动汽车的蓄电池靠工业电网充电,而太阳能汽车用的是太阳能电池。
(1)该太阳能汽车在白天给蓄电池充电的同时行驶,该行驶过程中首先_____能转化为化学能,然后转化为_____能,最终转化为机械能。
(2)该汽车车体主体材料是一种密度小、且抗腐蚀性好的一种合金,你认为下列材料中最合适的是_____(填字母)
A 玻璃钢 B 锰钢 C 硬铝 D 生铁
(3)目前还有一种新能源汽车,氢燃料电池汽车,该种汽车的储氢材料是循环吸放氢过程中生成新的氢化物,其中一种为氢化铝锂(LiAlH4)的氢化物,在125℃ 时分解为氢气和一种金属单质及氢化锂(LiH)。请你写出氢化铝锂分解反应的化学方程式①_____。反应前后铝元素的化合价分别为②_____。生活中使用的干电池中含有铅、镉、汞等,如果将废旧电池随意丢弃会③_____,威胁④_____。
【答案】光 电 C 2LiAlH4![]() 2Al+2LiH+3H2↑ +3、0 造成水体和土壤污染 人类健康
2Al+2LiH+3H2↑ +3、0 造成水体和土壤污染 人类健康
【解析】
(1)该太阳能汽车在白天给蓄电池充电的同时行驶,该行驶过程中首先光能转化为化学能,然后转化为电能,最终转化为机械能。故填:光;电;
(2)硬铝是一种密度小、且抗腐蚀性好的一种合金;故选:C;
(3)氢化铝锂(LiAlH4)在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH),反应方程式为:2LiAlH4![]() 2Al+2LiH+3H2↑;反应前LiAlH4中铝元素的化合价为+3价,反应后金属铝的化合价为0;生活中使用的干电池中含有铅、镉、汞等,如果将废旧电池随意丢弃会造成水体和土壤污染,威胁人类健康。故填:2LiAlH4
2Al+2LiH+3H2↑;反应前LiAlH4中铝元素的化合价为+3价,反应后金属铝的化合价为0;生活中使用的干电池中含有铅、镉、汞等,如果将废旧电池随意丢弃会造成水体和土壤污染,威胁人类健康。故填:2LiAlH4![]() 2Al+2LiH+3H2↑;+3、0;造成水体和土壤污染;人类健康。
2Al+2LiH+3H2↑;+3、0;造成水体和土壤污染;人类健康。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:初中化学 来源: 题型:
【题目】用化学符号和化学式表示:两个亚铁离子_____;氧化铁中铁元素化合价_____;磁铁矿的主要成分_____;儿童缺少_____元素严重时,会得佝偻病。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种物质在水中的溶解度曲线。以下说法正确的是( )
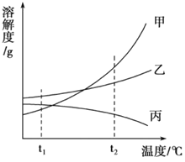
A. t2℃时溶解度由大到小的顺序是乙>丙>甲
B. 由t2℃降到t1℃析出晶体最多的是甲溶液
C. 由t2℃降到t1℃丙溶液浓度一定不发生变化
D. 甲乙丙三种物质溶解度都随温度升高而增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列重要实验,回答问题:
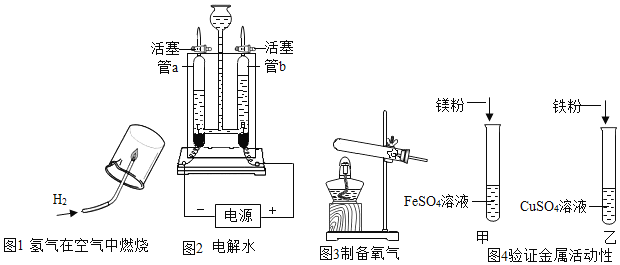
(1)图1所示实验中,观察到的现象是__________。
(2)图2所示实验,在电解器玻璃管里加满含有硫酸钠的水溶液(硫酸钠只增强导电性,不发生反应)玻璃管b内产生约l0mL气体时,玻璃管a内产生约______ mL气体。若取60g质量分数为1%的硫酸钠溶液进行电解, 消耗了l0g 水,则电解后硫酸钠溶液中溶质的质量分数为_________。
(3)图3用于实验室制备氧气,反应的化学方程式为_____________试管口放置棉花的目的是__________。
(4)图4实验得出的结论是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列应用及相应原理(用化学方程式表示)及基本反应类型均正确的是( )
A.用铁桶盛装波尔多液 Fe+CuSO4=FeSO4+Cu 置换反应
B.正常雨水显酸性 CO2+H2O=H2CO3 化合反应
C.用澄清石灰水吸收二氧化碳 CO2+Ca(OH)2=CaCO3↓+H2O 复分解反应
D.实验室制氧气 2KClO3=2KCl+3O2 分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】侯氏制碱法制得的纯碱样品中常含有少量氯化钠,为测定一份纯碱样品中碳酸钠的含量(假设样品只有碳酸钠和氯化钠组成),做如下实验:
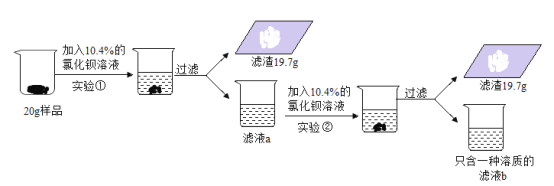
(1)上述实验过程中发生反应的化学方程式为_____;
(2)根据已知条件列出实验①中参加反应的碳酸钠质量(x)的比例式_____;
(3)样品中碳酸钠的含量为_____;
(4)两次实验消耗的氯化钡溶液的质量最简比为_____;
(5)若实验所用的氯化钡溶液是在其浓溶液中加入200g水稀释而来的,则稀释前溶液的浓度为_____;
(6)实验结束后,向滤液b中加入14.4g水,所得溶液中溶质的质量分数为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类是学习化学常用的方法。复分解反应发生是需要满足一定条件的,酸、碱、盐之间只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
请判断下列物质之间能否发生复分解反应,并根据不能发生反应的原因进行分类,参照实例完成下列内容:
①BaCl2+H2SO4﹣﹣
②KNO3+H2SO4﹣﹣
③NaCl+Cu(OH)2﹣﹣
④CaCO3+HCl﹣﹣
⑤NaC1+Ca(OH)2﹣﹣
⑥BaSO4+AgNO3﹣﹣

________;_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸、氢氧化钾、氯化钠是重要的化工原料,也是实验室常见的试剂。
(1)下列关于硫酸的说法不正确的是_____。
A 浓硫酸是粘稠、油状的液体
B 稀硫酸可用于铁制品除锈
C 浓硫酸滴到白纸上,使纸变黑
D 浓硫酸敞口放置,质量分数变大
写出上述选项中涉及到的化学方程式_____。
(2)氢氧化钾的化学性质和氢氧化钠相似。小兰在实验室内发现一瓶敞口久置的氢氧化钾溶液,她取出一部分,滴入稀盐酸后有气泡生成,请写出与发生此现象有关的两个化学方程式_____。
(3)从海水中晒出的粗盐中含有CaCl2、MgCl2、Na2SO4等可溶性杂质。为了除去杂质,有如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。
①加入Na2CO3溶液的目的是什么_____?
②这个过程中发生的复分解反应一共有几个_____?
③最终所得的氯化钠的质量和原来粗盐中含有的氯化钠的质量相比,有什么变化_____?
(4)小明在家里发现了一瓶食盐水,小明想测量这瓶食盐水中氯化钠的质量分数,取130g食盐水,加入足量硝酸银溶液,充分反应后,生成2.87g白色沉淀。求食盐水中氯化钠的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学课堂围绕“酸碱中和反应”,将学生分成若干小组探究。请你和他们一起完成以下实验探究。
(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是:_________,该反应的化学反应基本类型是_____。
(查阅资料)CaCl2溶液显中性
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想 I:只有 CaCl2 猜想 II:有_____
猜想 III:有 CaCl2 和 Ca(OH)2 猜想 IV:有 CaCl2、HCl 和 Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想 IV 不合理,其理由是_____。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入 CO2 | 滴加 Na2CO3 溶液 |
实验操作 |
|
|
|
实验现象 | ______ | _____ | 产生白色沉淀 |
实验结论 | 溶液中含有:Ca(OH)2 | 溶液中含有:Ca(OH)2 | 溶液中含有:Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想 III 是正确的。
(评价反思)
(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_____。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com