
已知胆矾溶于水时溶液温度降低。胆矾分解的热化学方程式为CuSO4·5H2O(s)===CuSO4(s)+5H2O(l) ΔH=+Q1 kJ·mol-1。室温下,若1 mol无水硫酸铜溶解为溶液放热Q2 kJ,则( )
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法比较
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小军很感兴趣,于是,他和同学们进行探究。
[提出问题]过氧化钠与水反应生成了什么物质?
为什么脱脂棉会燃烧?
 [猜想]①可能有一种气体和另一种物质生成
[猜想]①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
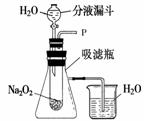
[设计装置]如右图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
⑴打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是 。
⑵实验中,还观察到伸入烧杯中的导管口有气泡冒出,
请解释产生该现象的原因:
实验二:继续探究反应后生成的另一种是什么?
⑴小张猜想另一种物质是Na2CO3,小军认为不可能。小军的依据是:
为了证实小军的看法,请你设计一个证明CO32-不存在的实验。(2分)
| 实验步骤 | 实验现象 | 实验结论 |
⑵小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈 性。
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式
查看答案和解析>>
科目:初中化学 来源: 题型:
Ⅰ.利用海水淡化后母液中含有的氯化镁和海边盛产的贝壳(主要成分CaCO3),制取金属镁,生产大致流程如下图所示:
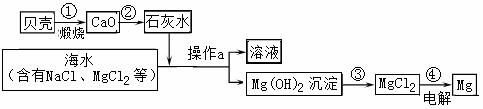
(1)请写出母液中氯化镁转化为氢氧化镁的化学方程式: 。
(2)操作a的名称是____________。
(3)工业上常以氯化镁为原料,电解就可以生产金属镁 。反应的化学方程式为MgCl2
。反应的化学方程式为MgCl2 Mg+X。X的化学式是_______。
Mg+X。X的化学式是_______。
Ⅱ.阅读下列两段材料,回答问题:
材料一:1811年法国药剂师库特瓦首次发现单质碘。单质碘呈紫黑色晶体,易升华,升华后易凝华。有毒性和腐蚀性。碘单质遇淀粉会变蓝紫色,可以用作鉴别淀粉的定量和定性的方法。人们可以从海藻中提取碘,也可以从智利硝石、生硝、海水、盐井中获得。
 材料二:碘元素在周期表中信息如图3所示。生活中将碘(I2)溶解在酒精中配
材料二:碘元素在周期表中信息如图3所示。生活中将碘(I2)溶解在酒精中配
制成碘酒,用于消毒;在食盐中加入碘酸钾(KIO3)制成碘盐,用于预防碘缺乏病。
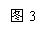 但碘酸钾与氯酸钾相似,加热会分解,生成碘化钾和氧气。
但碘酸钾与氯酸钾相似,加热会分解,生成碘化钾和氧气。
(1)碘属于 元素(填“金属”或“非金属”)。
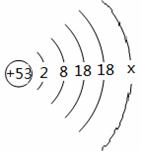 (2)碘原子的结构示意图如图4所示,推算x= ,在化学反应中
(2)碘原子的结构示意图如图4所示,推算x= ,在化学反应中
容易 电子(填“得”或“失”),形成的微粒符号是______。
(3)根据上述材料,总结下列有关知识:
碘的物理性质(写一点) ;
碘酸钾的化学性质(用化学方程式表示) ;
 烧菜使用加碘盐要注意 。
烧菜使用加碘盐要注意 。
查看答案和解析>>
科目:初中化学 来源: 题型:
向1.0 L 0.30 mol·L-1的NaOH溶液中缓慢通入8.8 g CO2气体,使其完全反应,对反应后的溶液,下列判断正确的是( )
A.溶质为Na2CO3
B.溶质为NaHCO3
C. c(Na+)=c(HCO
c(Na+)=c(HCO )+c(CO
)+c(CO )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO )+2c(CO
)+2c(CO )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:初中化学 来源: 题型:
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为
________________________________________________________________________。
(2)B为0.1 mol·L-1的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表
示)________________________________________________________________________
________________________________________________________________________。
(3)C为0.1 mol·L-1的(NH4)2Fe(SO4)2溶液,与同浓度的(NH4)2SO4溶液中相比较______(填溶质的化学式)溶液中NH 的浓度更大,其原因是
的浓度更大,其原因是
________________________________________________________________________
________________________________________________________________________。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:AgCl(s)
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25 ℃时,AgCl的Ksp=1.8×10-10mol2·L-2。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol·L-1 AgNO3溶液 ③100 mL 0.1 mol·L-1 MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为______(填序号),此时溶液②中Cl-物质的量浓度为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质溶液的燃料电池中发电,电池负极反应式为( )
A.H2+2OH--2e-===2H2O B.O2+4H++4e-===2H2O
C.H2-2e-===2H+ D.O2+2H2O+4e-===4OH-
查看答案和解析>>
科目:初中化学 来源: 题型:
)某学习小组设计以下实验,探究化学反应中的热效应,把试管放入盛有25 ℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管向其中滴加5 mL盐酸。试回答下列问题:

(1)实验中观察到的现象是________________________________________________________________________
________________________________________________________________________。
(2)产生上述现象的原因是________________________________________________________________________
________________________________________________________________________。
(3)写出有关反应的离子方程式:________________________________________________________________________。
(4)由实验推知,MgCl2和H2的总能量______(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
(5)如果将本题中“25 ℃的饱和石灰水”换成“20 ℃碳酸饮料”进行实验探究,实验中观察到的另一现象是______________________________________________________,
其原因是____________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
如图所示的装置中铁棒上析出铜,而铁的质量不变,符合要求的原电池是
( )。

A.铁棒作负极,铜棒作正极,电解质溶液是CuSO4溶液
B.镁棒作负极,铁棒作正极,电解质溶液是CuSO4溶液
C.镁棒作负极,铁棒作正极,电解质溶液是FeCl3溶液
D.铁棒作负极,铜棒作正极,电解质溶液是H2SO4溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
下列事实,不能用勒夏特列原理解释的是( )
A.氨水中加酸,NH的浓度增大
B.合成氨工业中不断从反应混合物中液化分离出氨气
C.实验室中常用排饱和食盐水的方法收集Cl2
D.合成氨温度控制在500 ℃左右
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com