
����Ŀ��ijͬѧ���������ͼ��ʾ��װ�ã�����ʵ������ȡ CO2�������IJ������ʽ���̽������Ҫ����⡣
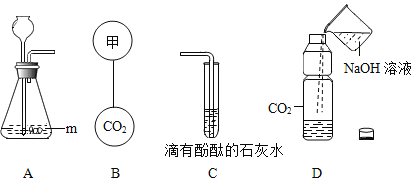
��1������ m ��������_____��A ������Ӧ�Ļ�ѧ����ʽΪ_____
��2����Ҫ B ���������������ڿ����������������_____������ţ�
A ���� B ���� C ����
��3����ͼ C �е��Թ�ͨ�� CO2��������_____������ʯ��ˮ�����ʸպ���ȫ������
��4���� D ��������ƿ��һ������ NaOH ��Һ��Ѹ��š��ƿ�棬���ɹ۲쵽ƿ�ӱ����ʹ������ƿ�ָ�ԭ״������ע������ƿע������_____�����Ա����ƣ���ַ�Ӧ���ɡ�
���𰸡���ƿ CaCO3+2HCl=CaCl2+CO2��+H2O C ��Һ��ɫ�ɺ�ɫ��Ϊ��ɫ ϡ����
��������
��1������m������Ϊ��ƿ��ʵ����������CO2���õķ�Ӧ����CaCO3��HCl������ʽΪCaCO3+2HCl=CaCl2+CO2��+H2O
��2��Ҫ�����������ڿ��м�Ҫ�����������γɵĵ���ϵƽ�⣬CO2���ܶȴ��ڿ����������ڿ����л��³�����˼�����������ܶ�С�ڿ������ۺ�����ѡ�ֻ��H2��������
��3��ʯ��ˮ������ΪCa(OH)2���Լ��ԣ���ʹ��̪��Һ��죬��CO2����Ca(OH)2��Ӧ����CaCO3��������Ca(OH)2�ܽ������ϼ��٣�����Ӧ��ȫʱ����Һ����Ca(OH)2����Һ�����ɫ����˴����Һ��ɫ�ɺ�ɫ��Ϊ��ɫ��
��4��ƿ�ӱ������ΪCO2��NaOH��Ӧ����Na2CO3����С��ƿ�ڵ�ѹǿ������ֻҪ�ܽ�CO2�ٷ�Ӧ��������������ƿ��ԭ���ܸ�Na2CO3��Ӧ����CO2�ľ��Ǽ����ϡ���ᡢϡ���ᡢϡ�������ᣬ��������һ���ɡ�
�ʴ�Ϊ��ƿ��CaCO3+2HCl=CaCl2+CO2��+H2O��C����Һ��ɫ�ɺ�ɫ��Ϊ��ɫ��ϡ����


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һʵ����ʵ������������ͭ��Һ��Ӧ��������ͭ���ɣ������н϶�����������Ϊȷ������ijɷ֣���������ʵ��̽����
��һ��̽�������������Ԫ�ؽǶȷ��������������SO2��O2��H2�е�һ�ֻ��֡�
������ʵ�飺
��1����ͬѧΪȷ���Ƿ���SO2����ͨ���������ϵ�֪��SO2��ʹ���Ը��������Һ��ɫ�����ǽ�����ͨ�����Ը��������Һ�У���Һ��ɫδ�����仯�����������_____SO2����������������������
��2����ͬѧ��Ϊֻ��O2���������_____�����顣ʵ��֤����ͬѧ�Ĺ۵㲻��ȷ
��3����ͬѧΪ�ж��Ƿ���O2��ͬʱȷ������ɷ֣�ͨ���������ϵ�֪���������ⵥ�ʻ����ɫ�� O2+4KI+4HCl��2I2+4KCl+2H2O��I2Ϊ�ⵥ�ʡ���������������µ�ʵ��װ�ã�
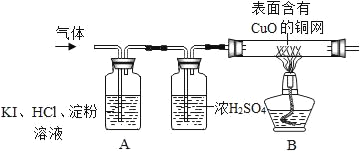
������ʵ����������ۣ�A�й۲쵽_____��֤����O2��B�й۲쵽_____��֤����������H2��
���ģ�ʵ�鷴˼��
��4�������Ϊ��ͬѧ�ڼ���֮ǰ��Ӧ��������_____��ȷ����ȫ��
��5��������ʵ���֪������ͭ��Һ��_____�ԣ���������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ǿ�ѧ̽������Ҫ;����

��1����ͼ��ʵ��������ȡ���峣�õ�����������ش��������⣺
����д����Dװ����ȡ�����Ļ�ѧ����ʽ��_____��
��ʵ���ҿ���̼���ƣ�CaC2�������ˮ��Ӧ����ȡ��Ȳ��C2H2�����壬�÷�Ӧ�����ϸ���Ƽ�ˮ�����ʣ�������ҷ�Ӧ����������װ��ը�ѣ�����ȡ��Ȳ�����ʺϷ���װ����_____������Eװ�ò�����ˮ�����ռ���Ȳ���������������______��
��2��ij��ѧ��ȤС���������ͼ��ʾ����ʵ�顣
�����������м���̼��ƣ���ѹ��Һ��������������ϡ���ᣬ���û�ѧ����ʽ��ʾ�䷴Ӧԭ��______��
�����������еķ�Ӧֹͣ���Թ�����Һ�������������У�����Ͳ�������������ܵ�ԭ��________��
����μ����Թ���ʣ����Һ�����������ƣ����Ҫд��ʵ�鲽�衢����ͽ���_________��
��3����Ȳ��C2H2����һ����Ҫ�Ļ���ԭ�ϣ�����̼���ƣ�CaC2����ˮ��Ӧ��ȡ��Ȳ��ͬʱ�����������ơ���Ҫ��ȡ7.8g��Ȳ���壬��������Ҫ̼���Ƶ������Ƕ���_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������һ������ͭ����Ʒ��ĩ�����п��ܻ�����п�����е�һ�ֻ��������ʡ���ѧ��ȤС��ͬѧ�������Ʒ����������ʵ�顣
ʵ��1����ȷ����Ʒ�ɷ�
��1������������1����ƷΪͭ��п
����2����ƷΪͭ����
����3����ƷΪͭ��_____�������ƣ�
��2���ô�����������Ʒ���۲쵽_____����С����ޡ������屻�����������1��������
��3��Ҫ����֤������Ʒ�ɷ֣���ȡ��Ʒ�������Թ��У�Ӧ�����ҩƷΪ_____������ţ���
A������þ��Һ B����������Һ C������п��Һ D������������Һ
�۲�ʵ����������ȷ������ƷΪͭ��������
ʵ��2������Ʒ����̽����������Ʒ���������������Һ��ϡ���ʵ��ⶨ����Һ�����淴Ӧʱ��仯�������ͼ��ʾ������˵���������_____������ţ���

A��a����Һ�е���������������������ͭ��������
B��b��������������֣���Һ�е�����������
C��ͼ��bc�η�������ͭ����������Һ�ķ�Ӧ
D��c���d���������������ͬ����Һ�е�����������ͬ
ʵ��3�����ⶨ����Ʒ��ͭ����������
���裺����ȡag��Ʒ�����ձ�����������ϡ���ᡣ
��ȡһ������Ϊbg����ֽ����������װ�ù�������
�������з�Ӧ��ֺ��ˡ�
��ȡ������ͬ��ֽ��ɡ�����������Ϊcg��
�ش��������⣺
��1������ʵ��������õ��IJ����������ձ�����ͷ�ιܡ�_____���������ȡ�
��2��ͨ������ʵ������Ʒ��ͭ������������_____����a��b��c��ʾ����
��3��С���ⶨ������ƫ���ܵ�ԭ����_____ ������ţ���
A������ʱ��©����Һ�������ֽ����
B��������֮�䣬ȱ��ϴ�������IJ���
C������ʱ����ҩƷ������ŷ��ˣ��ٶ�ֻ�в���������ʱʹ�������룩
D�������������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ����������ʵ�ת����ϵ����ͼ��ʾ����������ʾ��Ӧһ��ʵ�֣��������ʺͷ�Ӧ��������ȥ��������ѡ���ʵ��ͼʾת������
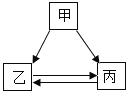
ѡ�� | �� | �� | �� |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Ca(OH)2 | CaCl2 | CaCO3 |
D | NaOH | NaCl | NaNO3 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʯ��ʯ����Ҫ�ɷ� CaCO3��������ʯ�ң�CaO���Ͷ�����̼��Ϊ�˲ⶨijʯ��ʯ��̼��ƣ�CaCO3���ĺ������ֳ�ȡ 24.0g ʯ��ʯ��Ʒ�������Ĵθ������ա���ȴ������ʣ���������� �����ʲ��μӷ�Ӧ������¼ʵ���������£�
���� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
ʣ��������� | 21.6g | 19.2g | 15.2g | 15.2g |
�Լ��㣺
��1����ȫ��Ӧ�����ɶ�����̼������Ϊ_____��
��2�����ʯ��ʯ��Ʒ��̼��Ƶ�����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ��һ����������������ģ�����Ӧ���˽�һЩ�й�ˮ��ˮ��Һ�����֪ʶ��
��1��Ӳˮ����������������ܶ��鷳�������п���________������Ӳˮ����ˮ������ˮ�Ļ�ѧ���ʵ�����___________���������ƣ���
��2��ij����ˮ�������к����������ۣ�����������������ˮ�е�ijЩ��Ⱦ�����������__________����������ƣ���ȥ����Ⱦ��������ƣ�Na2FeO4��Ҳ��һ�����͵ĸ�Ч��ˮ����������������Ԫ�صĻ��ϼ�Ϊ___________��
��3����ͼ������أ�KNO3�����Ȼ��ƣ�NaCl�����ܽ�����ߣ���ش�
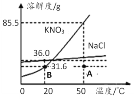
��50��ʱ��100gˮ���������ܽ�________g����ء�
��20��ʱ����100gˮ�м���35g����ع��壬��ֽ����������ҺΪ_____________��Һ������͡������͡�����������Һ���µ�50��ʱ��������������_______________��ֻ���б���ʽ������д���𰸣���
�۵�������л��������Ȼ���ʱ�����Բ���_____________�ķ����ᴿ����أ������������Һ��A��ת��ΪB�㣬�ɲ�ȡ�Ĵ�ʩ��________________________��
��20��ʱ����KNO3��NaCl�������ʵı�����Һ��100g���ֱ��������10gˮ����������϶����____________���KNO3����NaCl������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��a��b��c���ֹ������ʵ��ܽ������ͼ����ش����⣺
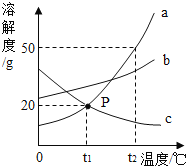
(1)t1��ʱ��a��b��c���������У��ܽ���ɴ�С��˳����______��
(2)��c���ʵIJ�������Һת��ɱ�����Һ�ɲ�ȡ�ķ�����______ (д��һ�ּ���)��
(3)t2��ʱ����30ga���ʼ���50gˮ�г���ܽ��������Һ��������______g��
(4)ͼ��P������ʾ��������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ĸ���ѧ��Ӧ�����п�����ͼģ��![]() ����ʾ�Ļ�ѧ��Ӧ�� �� ��
����ʾ�Ļ�ѧ��Ӧ�� �� ��
A. 2HgO=2Hg��+O2��B. 2HClO=2HCl+O2��
C. 2H2O=2H2��+O2��D. CaCO3=CaO+CO2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com