
| 问题与猜想 | 实验步骤 | 实验现象 | 结论、化学方程式 |
| 双吸剂是否失效 | 取样品少量于试管中加入适量的稀盐酸 | 产生大量气泡 | 结论:双吸剂没有失效,有关反应的化学方程式:Fe+2HCl═FeCl2+H2↑ |
分析 (1)根据题意,上网查阅包装袋内是纯度较高的铁粉,据此结合铁锈蚀的条件,进行分析解答.
(2)根据铁粉能增大与氧气、水分的接触面积,进行分析解答.
(3)实验探究“双吸剂”是否失效,即检验“双吸剂”中是否含铁,据此结合铁能与酸反应生成氯化亚铁和氢气,进行分析解答.
解答 解:(1)上网查阅包装袋内是纯度较高的铁粉,主要吸收空气中的两种物质是食物保鲜所以也称“双吸剂”,铁与氧气、水分接触容易生锈,则吸收的物质指的是氧气、水分,其化学式为O2、H2O.
(2)用铁粉而不用铁块作“双吸剂”,是因为能增大与氧气、水分的接触面积,加快反应速率.
(3)判断双吸剂是否失效,即检验“双吸剂”中是否含铁,取样品少量于试管中加入适量的稀盐酸,产生大量气泡,说明“双吸剂”中含有铁粉,双吸剂没有失效.铁能与酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:(1)O2、H2O;(2)增大与氧气、水分的接触面积,加快反应速率;(3)
| 问题与猜想 | 实验步骤 | 实验现象 | 结论、化学方程式 |
| 双吸剂是否失效 | 取样品少量于试管中加入适量的 稀盐酸 | 产生大量气泡 | 结论:双吸剂没有失效,有关反应的化学方程式:Fe+2HCl═FeCl2+H2↑ |
点评 本题难度不大,掌握铁生锈的条件、金属的化学性质、化学方程式的书写方法并能灵活运用是正确解答本题的关键.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:初中化学 来源: 题型:解答题

| 现象 | 解释 |
| A试管中白磷燃烧,热水中白磷没有燃烧 | 热水中白磷没有与氧气接触 |
| b试管中红磷没有燃烧 | 温度未达到红磷的着火点 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 小孩经常铅笔,会导致铅中毒 | B. | 久未开启的地窖,不可冒然进人 | ||
| C. | 加碘食盐的“碘”是指碘元素 | D. | 区别硬水与软水常用肥皂水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 选项 | 实验目的 | 实验设计 |
| A | 鉴别木炭分和氧化铜粉 | 取样后,混合均匀,高温加热 |
| B | 鉴别氧气和二氧化碳 | 闻气味 |
| C | 鉴别稀盐酸和稀硫酸 | 取样后,分别滴加氯化钡溶液,振荡 |
| D | 鉴别腈纶毛线和羊毛线 | 取样品,灼烧,闻气味 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用脱硫煤 | |
| B. | 加大城市绿化、道路定期洒水、控制工地扬沙 | |
| C. | 积极推行油品的升级 | |
| D. | 通过加高烟囱排放工业废气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 .钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目;银白色有金属光泽,钠还能与水反应,生成氢氧化钠和氢气.目前,世界上多数采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度.电解时,正极放出氯气,负极产生的金属钠和金属钙同时浮在共熔物,从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出,通过过滤可以分离出金
.钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目;银白色有金属光泽,钠还能与水反应,生成氢氧化钠和氢气.目前,世界上多数采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度.电解时,正极放出氯气,负极产生的金属钠和金属钙同时浮在共熔物,从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出,通过过滤可以分离出金| 原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 元素名称 | ||||||||||
| 元素符号 | ||||||||||
| 原子序数 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 元素名称 | ||||||||||
| 元素符号 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2016年3月5日,国务院总理李克强在2016年《政府工作报告》中指出,加强重大基础设施建设,到2020年高铁营业里程达到3万公里.而截至2015年底,国内高铁营运里程已经达到1.9万公里,也就是说需要在未来五年内新增1.1万公里.使人们的出行进入“高铁时代”.
2016年3月5日,国务院总理李克强在2016年《政府工作报告》中指出,加强重大基础设施建设,到2020年高铁营业里程达到3万公里.而截至2015年底,国内高铁营运里程已经达到1.9万公里,也就是说需要在未来五年内新增1.1万公里.使人们的出行进入“高铁时代”.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | K2SO4、NaCl、HCl | B. | HNO3、KOH、KMnO4 | ||
| C. | BaCl2、Na2SO4、NaOH | D. | Ca(NO3)2、Na2CO3、KCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
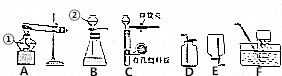
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com