
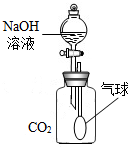
 在化学课上老师向NaOH溶液通入CO2后无明显现象.提出问题:如何通过实验证明CO2与NaOH发生了反应.
在化学课上老师向NaOH溶液通入CO2后无明显现象.提出问题:如何通过实验证明CO2与NaOH发生了反应.分析 根据氢氧化钠与二氧化碳的反应以及生成产物的检验进行分析解答,根据氢氧化钠溶液中的二氧化碳会对实验有影响要设计对照实验解答即可.
解答 解:【实验一】
(1)氢氧化钠吸收二氧化碳,导致装置内的压强变小,气球会鼓起来,故填:气球变鼓;
(2)由于氢氧化钠溶液中含有水,二氧化碳能溶于水使气体减少,也会使气球鼓起来,故需要设计对照实验,故填:二氧化碳能溶于水,也能使气球变鼓,不能证明二氧化碳与氢氧化钠发生了反应;设计对比试验,用同样体积的水与同样的二氧化碳,观察气球的形变.
【实验二】
(1)碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,故填:CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)方案一中若是有剩余的二氧化碳,则也能使澄清的石灰水变浑浊,故填:方案一;装置中有剩余的二氧化碳气体,能使澄清的石灰水变浑浊.
点评 掌握常见的碱的性质以及物质间反应的实验现象是正确解答本题的关键.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:选择题
| A. | 电解水实验中正极与负极产生的气体体积之比为4:1 | |
| B. | 硫粉在氧气中燃烧产生蓝紫色火焰 | |
| C. | 将铁钉浸到硫酸铜溶液中,铁钉表面会有红色固体生成,溶液变成无色 | |
| D. | 在氯化铜溶液中滴加氢氧化钠溶液,有白色沉淀生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
 某溶液中含有稀硫酸、碳酸钠、硫酸钠、盐酸、氯化镁、硝酸钾中的一种或几种,向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积之间的关系如图所示,则下列判断正确的是( )
某溶液中含有稀硫酸、碳酸钠、硫酸钠、盐酸、氯化镁、硝酸钾中的一种或几种,向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积之间的关系如图所示,则下列判断正确的是( )| A. | 该溶液中溶质的组成有二种情况 | |
| B. | 该溶液是否含氯化镁不能确定 | |
| C. | 该溶液中不可能含碳酸钠和硫酸钠 | |
| D. | 该溶液中含有盐酸或稀硫酸,也可能两种酸同时含有 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
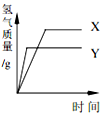 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中正确的是( )
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中正确的是( )| A. | 生成氢气的质量:X<Y | B. | 消耗硫酸的质量:X<Y | ||
| C. | 金属的活动性:Y<X | D. | 相对原子质量:X<Y |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com