
【题目】小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
【知识回放】金属活动性顺序:(请你在横线上填写所缺的金属的元素符号)
K Ca NaMg Al__FeSnPb(H) Cu Hg __Pt Au
【作出猜想】
猜想1:Fe>Cu>Cr
猜想2:Fe>Cr>Cu
(你的猜想)猜想3:________________。
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,在常温下分别放入等量的同种浓度的稀硫酸中。请填写试管3中的实验现象
实验 | 试管1 | 试管2 | 试管3 |
实验操作 |
|
|
|
实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | ________ |
【结论与解释】
(1)小聪得到的结论是猜想_________正确。
(2)实验前用砂纸打磨金属片的目的是___________________________________________。
【知识运用】将铬片投入FeSO4溶液中,反应________(填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式:___________
【答案】 Zn Ag Cr>Fe>Cu 没有明显变化(或没有气泡产生) 猜想3 除去金属表面的氧化膜,便于金属和稀硫酸顺利反应 能 Cr + FeSO4 == CrSO4 + Fe
【解析】(1)常见金属活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,故所缺金属为Zn和Ag;(2)三种金属的活动性顺序可能存在三种情况:猜想1为Fe>Cu>Cr;猜想2为Fe>Cr>Cu,故猜想3 Cr>Fe>Cu;(3)因为铜的活动性顺序位于氢的后面,因此不能和酸反应,表现为无现象;(4)试管1中实验现象铁片表面产生气泡较慢,溶液变为浅绿色,可知金属铁在金属活动顺序中排在氢前,根据铬片表面产生气泡较快,溶液变为蓝色,从而得出铬也排在氢前且铬比铁活泼,因为铜不能和稀硫酸反应生成氢气,可知铜排在氢的后面,故猜想3、Cr>Fe>Cu正确;(2)实验前用砂纸打磨金属片的目的是:除去金属表面的氧化膜,便于金属和稀硫酸顺利反应;(5)因为“铬片表面产生气泡较快溶液变为蓝色”,可知金属铬比铁活泼强,,故铬能和硫酸亚铁反应生成硫酸铬和铁,则反应的化学方程式为:Cr+FeSO4=Fe+CrSO4。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】乙硫醇(化学式为C2H6S)易挥发,有蒜臭味,人对该气味极其敏感,下列有关乙硫醇的说法不正确的是( )
A. 乙硫醇的相对分子质量为62
B. 乙硫醇中C、H、S三种元素的质量比是2: 6:1
C. 硫元素的质量分数是![]() ×100%
×100%
D. 在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是甲、乙两种物质的溶解度曲线。20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到图2所示的现象。下列说法正确的是
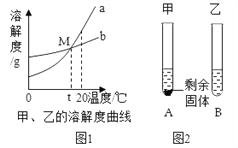
A. 20℃时,乙溶液是饱和溶液
B. t℃后乙溶解度大于甲的溶解度
C. 升高温度可使两试管中甲、乙溶液的质量分数均增大
D. 从20℃降低到t℃时,甲、乙两物质的溶解度相等,两试管中甲溶液溶质质量分数与乙溶液相等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线.
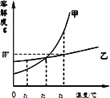
(1)t1℃时,甲的溶解度____乙的溶解度(选填“大于”“等于”或“小于”);
(2)要使接近饱和的甲溶液变为饱和溶液,可采取的方法是_________________(只填一种);
(3)甲、乙各Wg分别加入到两只盛有100g水的烧杯中,充分搅拌,在t3℃时所得乙溶液为______溶液(选填“饱和”或“不饱和”);若将温度都降低到t2℃,甲溶液中溶质的质量分数______乙溶液中溶质的质量分数(选填“大于”“等于”或“小于”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小刚同学在做一定溶质质量分数的氯化钠溶液的配制实验时,其配制过程如下图所示。
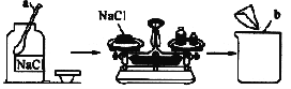
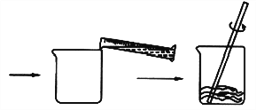
试回答下列问题:
(1)写出图中有标号仪器的名称:![]() ____________,
____________,![]() ____________。
____________。
(2)图示实验中有一处明显的错误是_______________________________________________;
图示实验中玻璃棒的作用是________________________________________________。
(3)小刚同学要配制90g质量分数为10%的氯化钠溶液,应称取氯化钠的质量为__________g,需要量取水的体积为________ml(水的密度近似看作1g/ml)。
(4)称量氯化钠时,若将氯化钠放在天平的右盘中,砝码放在天平的左盘中,并且在称量过程中使用了游码,则会使称取的质量________(填“大于”或“小于”)配制溶液所需的质量。
(5)在量取水的体积时,小刚同学俯视读数,则所配制溶液中氯化钠的质量分数________(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们学习”二氧化碳实验室制取的研究”课题时,探究了二氧化碳的收集方法。
(查阅资料)
(1)通常状况下 1 体积水约溶解 1 体积二氧化碳,所得溶液的 pH 约为 5.6,pH 越小,二氧 化碳在水中溶解越多。
(2)石灰石中的杂质既不和盐酸反应,也不溶于水。
(提出问题)二氧化碳能不能用排水法收集?
(设计实验) 实验一:在通常状况下,测定二氧化碳溶于水所得溶液的 pH,判断二氧化碳 在水中溶解的体积,如下图:
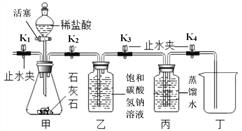
(1)甲装置中反应的化学方程式_____;
(2)检查甲装置气密性的方法是关闭活塞和止水夹 K1 ,打开 K2,K3,K4 双手握住锥形瓶, 观察到_____,说明装置气密性良好;
(3)实验时,需先将甲装置中的空气排尽。其操作是打开止水夹 K1,关闭止水夹 K2 ,打开 活塞,滴加稀盐酸至空气排尽。检验空气排尽的方法是 _____;
(4)关闭 K1 ,打开 K2 、K3 、K4 ,待丙装置中收集半瓶气体时,关闭 K2 、K3 、K4 ,充 分振荡丙装置,分别测得丙、丁瓶装置中溶液的 pH 为 5.5 和 6.5。分析可知,溶解的二氧化碳体积丙装置中_____(填“大于”或“等于”或“小于”)丁装置,乙装置的作用是 _____ ;
(5)实验结束后,装置甲反应后溶液中溶质除了氯化钙还有没有其他物质?请设计实验证明你的猜想(写出实验方法、现象和结论)______
(6)实验二:用二氧化碳数字传感器测得收集的气体中二氧化碳体积分数。如图是收集的 气体中二氧化碳体积分数随时间变化的关系图,从图中能得息:
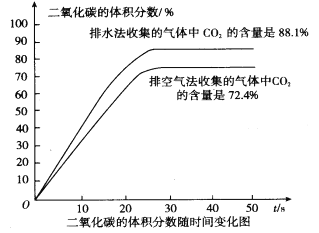
① ________________________________________
②___________________________________________________
(结论反思)由实验一、二分析,改进实验装置,二氧化碳能用排水法收集。能降低二氧 化碳在水中溶解性的措施③_____④_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料。某硫酸钠粗品中含有少量的氯化钙、氯化镁,实验室进行提纯的流程如下:
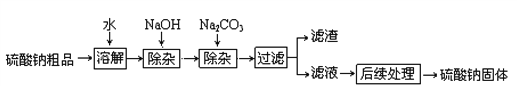
(1)滤渣中两种主要成分的化学式为 ________、____________。
(2)NaOH和Na2CO3如果添加过量了,可加入适量__________溶液除去。
(3)“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至______选填字母)。
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下:
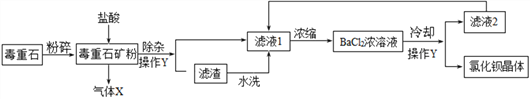
(1)操作Y的名称是_______,滤液2中可循环利用的物质除水外还有______。
(2)洗涤氯化钡晶体最适宜的洗涤剂是_______(填字母序号)。
A.20℃水 B.20℃饱和氯化钠溶液 C.20℃饱和氯化钡溶液
(3)现用25g毒重石(主要成分为BaCO3杂质不溶于水也不溶于酸)样品和100g溶质质量分数为7.3%的稀盐酸恰好完全反应。请通过计算:该毒重石中碳酸钡的质量分数是_______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】葡萄糖存在于葡萄糖汁和其他带甜味的水果里,是一种重要的营养物质,是人类生命活动所需能量的重要来源之一,下列关于葡萄糖的说法正确的是
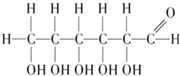
A. 葡萄糖分子中碳元素的质量分数最小
B. 葡萄糖的相对分子质量是180g
C. 葡萄糖分子中C、H、O三种元素的原子个数比为1 :2 :1
D. 葡萄糖是多原子分子构成的有机高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com