
分析 (1)根据用天平称量物体时的正确操作顺序进行分析解答;
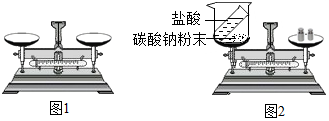
(2)铁与蓝色的硫酸铜溶液发生置换反应,生成硫酸亚铁溶于水中,同时生成红色固体铜,反应中没有气体参加,所以放在敞口的烧杯中进行实验,反应前后烧杯内物质质量也不变;
(3)碳酸钠与盐酸反应生成物中有气体二氧化碳,所以放在小烧杯内进行反应时,二氧化碳气体逸散到空气中,而使反应前后烧杯内物质的质量不相等;
(4)根据化学方程式和已知条件“C、D相对分子质量之比为15:9,若有1.7g A与B完全反应生成3g C”,列出比例式,即可求出D的质量,然后根据质量守恒定律计算出B的质量,进而计算出B和C的质量比.
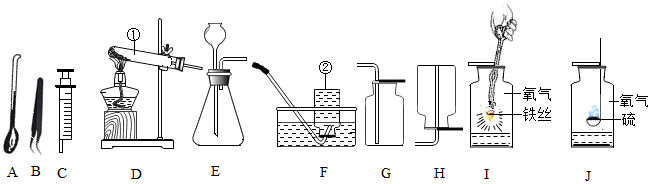
解答 解:(1)用天平称量物体时的正确操作步骤是:先调零点,然后在左右两盘中各方一张相同的纸,把称量物放到左盘,然后向右盘中放砝码,放砝码的顺序是先放质量大的,再放质量小的,最后用游码调平.故正确操作顺序为④②③⑤⑥①.
(2)铁与硫酸铜溶液发生置换反应,生成硫酸亚铁和铜.反应中没有气体参加,所以烧杯内物质的总质量始终不变.
(3)碳酸钠与盐酸生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;根据质量守恒定律,反应前各物质的总质量等于反应后各物质的总质量,但由于生成的二氧化碳气体放出,所以烧杯内物质的总质量随反应的发生不断减小.
(4)解:已知C和D的相对分子质量比为15:9,设生成D的质量为x,则
4A+5B═4C+6D
15×4 9×6
3g x
$\frac{15×4}{9×6}=\frac{3g}{x}$
x=2.7g
根据质量守恒定律可得参加应的B的质量=3g+2.7g-1.7g=4g;
则B和C的质量比为4g:3g=4:3.
故答案为:(1)B;
(2)=;
(3)Na2CO3+2HCl═2NaCl+H2O+CO2↑;>;生成的二氧化碳逸散到空气中,依据质量守恒定律,反应前烧杯中反应物的总质量大于反应后烧杯中剩余物的总质量;
(3)4:3.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.但要注意在任何与周围隔绝的体系中,不论发生何种变化或过程,其总质量始终保持不变.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用手拿着试管,给试管里的物质加热 | |
| B. | 用酒精灯引燃另一只酒精灯 | |
| C. | 用未经清洗的滴管去吸取别的试剂 | |
| D. | 给试管里的液体加热时,液体不超过试管容积$\frac{1}{3}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫铵、氢氧化钠两种固体研磨:(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑ 复分解反应 | |
| B. | 氢氧化钠吸收二氧化硫:2NaOH+SO2═Na2SO3+H2O 中和反应 | |
| C. | 碳还原氧化铁:2Fe2O3+3C$\frac{\underline{\;\;△\;\;}}{\;}$4Fe+3CO2↑ 置换反应 | |
| D. | 溶洞的形成:Ca(HCO3)2═CaCO3↓+H2O+CO2↑ 分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
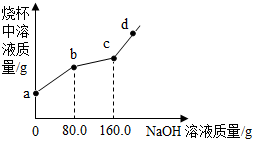 烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )| A. | ab段反应产生蓝色沉淀 | B. | bc段溶液增加70.2g | ||
| C. | c点对应的溶质质量分数为4.9% | D. | d点溶液中溶质有2中,且PH>7 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁粉 | B. | 紫色石蕊试液 | C. | K2CO3溶液 | D. | AgNO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 品红在热水中扩散比冷水中的快--水分子间有间隔 | |
| B. | 用水壶烧水,水开时壶盖被顶开--水分解生成氢气和氧气 | |
| C. | 在生煤火炉时,可点燃木柴来引燃煤--木柴的着火点比煤低 | |
| D. | 金刚石和石墨物理性质存在差异--构成它们的原子数目不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com