
| A. | 34% | B. | 48% | C. | 54% | D. | 68% |
分析 铝土矿的主要成分是氧化铝,在高温条件下能和氢气反应生成铝和水,铝能和稀硫酸反应生成硫酸铝和氢气,根据提供的数据可以进行相关方面的计算.
解答 解:设铝的质量为x,
2Al+3H2SO4═Al2(SO4)3+3H2↑,
54 294
x 98g×20%
$\frac{54}{x}$=$\frac{294}{98g×20%}$,
x=3.6g,
氧化铝的质量为:3.6g÷($\frac{54}{102}$×100%)=6.8g,
则此铝土矿的纯度为:$\frac{6.8g}{6.8g+3.2g}$×100%=68%,
故选:D.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.


科目:初中化学 来源: 题型:解答题
| 物质序号 | 甲 | 乙 | 丙 | 丁 |  |
| 微观 示意图 |  |  |  |  | |
| 反应前质量/g | 68 | 100 | 1 | 0 | |
| 反应后质量/g | 0 | x | y | z |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
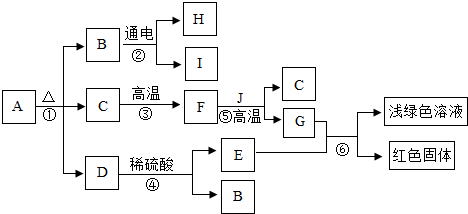
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
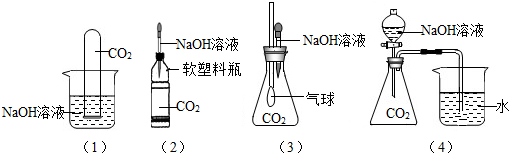
 利用CO2催化氢化可制CH4,其实验流程如图所示.
利用CO2催化氢化可制CH4,其实验流程如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁 | B. | 铝 | C. | 锌 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
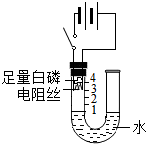 (1)在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水.哪些因素还能影响过氧化氢分解的速率?课外活动小组对此进行了更深入的探究:
(1)在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水.哪些因素还能影响过氧化氢分解的速率?课外活动小组对此进行了更深入的探究:| 实验步骤 | 现象 | 结论 |
| 取一支试管加入3~5mL5%的过氧化氢溶液,然后加入少量二氧化锰 | 有少量气泡缓慢冒出 | |
| 另取一支试管加入3~5mL15%的过氧化氢溶液,然后加入少量二氧化锰 | 有大量气泡迅速冒出 |
| 实验步骤 | 现象 | 结论 |
| 温度越高,过氧化氢分解的速率越大 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图用于研究CO2密度大于空气且能与水反应的性质,其中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.
如图用于研究CO2密度大于空气且能与水反应的性质,其中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com