
分析 根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
根据提供的数据可以进行相关方面的计算;
碱石灰能够吸收水蒸气和二氧化碳.
解答 解:(1)镁在氮气中燃烧生成氮化镁的化学方程式为:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;氮化镁与水反应的化学方程式为:Mg3N2+6H2O═3Mg(OH)2+2NH3↑;
(2)设12g镁和氧气反应生成的氧化镁的质量为x,12g镁和氮气反应生成氮化镁的质量为y,
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,
48 80
12g x
$\frac{48}{12g}=\frac{80}{x}$
x=20g
3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2,
72 100
12g y
$\frac{72}{12g}=\frac{100}{y}$
y≈16.67
(3)
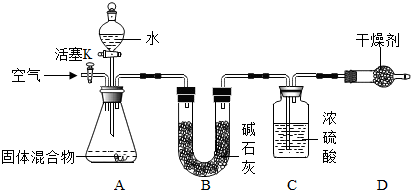
①装置B的作用是吸收水蒸气;
②装置D的作用是防止空气中的水蒸气进入C装置中;
③实验步骤④中鼓入空气的目的是使生成的氨气完全被浓硫酸吸收;
④设氮化镁的质量为z,
装置C增重0.34g,说明生成了0.34g氨气,
Mg3N2+6H2O═3Mg(OH)2+2NH3↑,
100 34
z 0.34g
$\frac{100}{z}=\frac{34}{0.34g}$
z=1g,
固体混合物中Mg3N2的质量分数为:$\frac{1g}{5g}$100%=20%;
⑤实验证明此方法测定的结果偏低,可能原因是部分氨气溶于水中.
答案:
(1)3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑;
(2)20; 16.67;
(3)①吸收水蒸气; ②防止空气中的水蒸气进入C装置中; ③使生成的氨气完全被浓硫酸吸收;④20%; ⑤部分氨气溶于水中.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
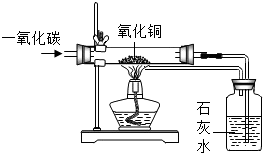 符合如图所示装置的选项是( )
符合如图所示装置的选项是( )| A. | ①② | B. | ①②③ | C. | ②③④ | D. | 全部 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
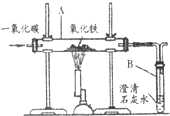 如图是一氧化碳还原氧化铁的炼铁原理示意图.请回答下列问题:
如图是一氧化碳还原氧化铁的炼铁原理示意图.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com