
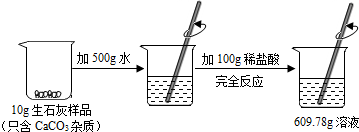
分析 由于碳酸钙与稀盐酸反应生成了二氧化碳气体,根据反应前后的质量差可以求出生成二氧化碳的质量,根据二氧化碳的质量可以求出碳酸钙的质量,再求出样品中CaCO3的质量分数.
解答 解:(1)反应前后的质量差即是生成的二氧化碳的质量,生成的二氧化碳的质量为:10g+500g+100g-609.78g=0.22g,
(2)设样品中CaCO3的质量为X,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
X 0.22g
$\frac{100}{44}=\frac{X}{0.22g}$ 解得:X=0.5g,
样品中CaCO3的质量分数为:$\frac{0.5g}{10g}$×100%=5%.
答:(1)生成CO2气体的质量为0.22g;(2)样品中CaCO3的质量分数为5%.
点评 解答本题关键是要能够通过反应前后的质量差,求出生成的二氧化碳的质量,其它计算就迎刃而解了.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
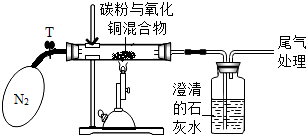 某小组同学对木炭还原氧化铜实验进行如下探究活动.
某小组同学对木炭还原氧化铜实验进行如下探究活动.| 木炭与氧化铜的质量比 | 1:7 | 1:11 | 1:13 |
| 实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,有气泡,石灰水变浑浊 |
| 实验结果 | 表层铜珠较大,有较多黑色粉末 | 亮红色金属光泽,网状铜块 | 暗红色层状粉末里含微细铜粒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 45.8 | 85.5 | 110 | 138 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com