
如果将装有浓硫酸和浓盐酸试剂瓶分别敞口放置在空气中一段时间后,浓硫酸的质量将会________,浓盐酸的溶质质量分数将会________(填“增加”、“减小”或“不变”)
 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:阅读理解

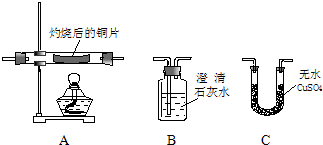
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| △ |

| 实验序号 | l | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 铁的氧化物质量(g) | 4.00 | 8.00 | 10.00 | 12.00 | 14.00 | 16.00 | 18.00 | 20.00 |
| 生成铁的质量(g) | 2.8l | 5.62 | 7.01 | 8.42 | 9.81 | 11.22 | 12.63 | 14.03 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2013?井研县模拟)某初三化学兴趣小组成员在购回的袋装薯片中发现还有一个小袋,上面标有如右图信息.撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是白色的.经过同学们分析讨论,认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe.为了验证自己的判断,他们进行了以下实验探究,请你一同参与.
(2013?井研县模拟)某初三化学兴趣小组成员在购回的袋装薯片中发现还有一个小袋,上面标有如右图信息.撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是白色的.经过同学们分析讨论,认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe.为了验证自己的判断,他们进行了以下实验探究,请你一同参与.查看答案和解析>>
科目:初中化学 来源: 题型:
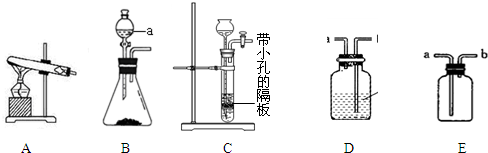
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com