
【题目】下表为KCl、NaCl和KNO3在不同温度时的溶解度,如图为它们的溶解度曲线. 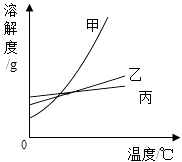
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | KCl | 34.0 | 37.0 | 42.6 | 45.5 | 51.1 |
NaCl | 36.0 | 36.3 | 37.0 | 37.3 | 38.4 | |
KNO3 | 31.6 | 45.8 | 85.5 | 110.0 | 169.0 | |
(1)30℃时,KCl的溶解度为 .
(2)如图中表示KNO3溶解度曲线的是(填“甲”、“乙”或“丙”).
(3)30℃时,向45.8g KNO3固体中加入100g水,充分溶解后升温至40℃,该溶液中溶质的质量分数(填“变大”、“变小”或“不变”).
(4)要将丙的不饱和溶液转化为饱和溶液适宜的方法是 .
【答案】
(1)36.0g
(2)甲
(3)不变
(4)蒸发结晶
【解析】解:(1)根据表中的信息可确定 30℃时KCl的溶解度为37.0g;所以答案是36.0g(2)根据表中的信息可确定硝酸钾的溶解度随温度变化明显,而氯化钾的溶解度随温度变化很不明显,所以答案是:甲;(3)30℃时KNO3的溶解度为45.8g,100g水中最多溶解45.8g,向45.8g KNO3固体中加入100g水,恰好完全溶解,由于硝酸钾的溶解度随温度的升高而增大,升温至40℃,变为不饱和溶液,溶质质量和溶剂质量不变,该溶液中溶质的质量分数不变;(4)丙的溶解度随温度变化不大,将丙的不饱和溶液转化为饱和溶液适宜的方法是蒸发结晶. 答案:(1)36.0g(2)甲(3)不变(4)蒸发结晶
【考点精析】解答此题的关键在于理解饱和溶液和不饱和溶液相互转变的方法的相关知识,掌握饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂,以及对固体溶解度曲线及其作用的理解,了解1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
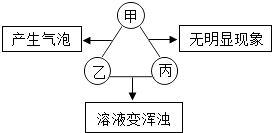
【题目】如表所列各组物质中,符合图示甲、乙、丙两两混合后发生反应的实验现象的是
甲 | 乙 | 丙 | |
① | 盐酸 | Na2CO3溶液 | Ca(OH)2溶液 |
② | 盐酸 | K2CO3溶液 | CaCl2溶液 |
③ | 盐酸 | K2CO3溶液 | Ba(OH)2溶液 |
④ | 盐酸 | Na2CO3溶液 | BaCl2溶液 |
( )
A.①②
B.③④
C.①③
D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种物质的溶解度曲线: 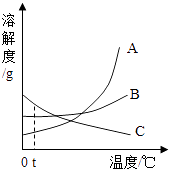
(1)t℃时,溶解度排第二物质是(填字母);
(2)要使不饱和的A溶液变为饱和溶液,最可靠的办法是(请选择下列答案序号填空); a.升温 b.加A物质 c.加溶剂
(3)溶解度随温度升高而减小的物质是(填字母).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D都是九年级化学中常见的物质,它们存在右下图所示的关系(反应条件略去). 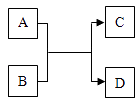
(1)若A为常见金属,C为气体单质,B的化学式为 , D的物质类别是(填酸、碱、盐、氧化物).
(2)若A为实验室常用燃料,C为植物光合作用所需的气体,则B的化学式为;D的名称为 .
(3)若A为非金属氧化物,C为红色固体,写出A与 B反应的化学方程式 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2012年6月1日,南宁市召开了环境质量状况新闻发布会.其中1~5月的检测结果表明,南宁的主要江河水质总体良好,邕江5个地表水水源地的水质达标率为100%.
(1)地表水水源地取出的天然水常携带有树叶等不溶性杂物,可利用沉淀、、吸附和蒸馏等方法进行净化,其中净化程度最高的方法是 .
(2)南宁市郊一些村庄的饮用水是从深井取用的地下水.取适量地下水,加入并搅拌,若观察到水中起浮渣,则证明从深井取用的地下水是(填“硬水”或““软水”).日常生活中常用的方法来降低水的硬度.
(3)氧气在自然界中存在非常广泛,并不断循环转化.氧元素在①人体,②海水,③空气,④地壳四种体系中,质量分数最高的是(填序号).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A~H是初中化学中的常见物质,它们之间的互相转化关系如图(1)所示.A、H为气体单质,且A是标准状况下密度最小的气体,E、F是两种生活中常见的盐(图中“→”、“←”表示物质间的转化,反应条件及部分反应物、生成物已省略). 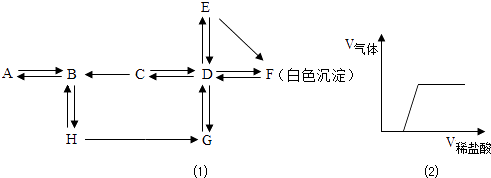
(1)A是 , F是 . (填化学式)
(2)B→H反应的化学方程式是 , 其基本反应类型是 .
(3)D→G反应的化学方程式是 .
(4)E→F反应中可观察到有白色沉淀产生,充分反应后过滤,向滤液中滴加稀盐酸,产生气体体积与所加稀盐酸体积的关系如图(2)所示.由此可推知上述滤液中含有的溶质是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是100g某品牌板栗的部分营养成分.
总热量 | 蛋白质 | 糖类 | 油脂 | 钠 | 维生素C |
1016kJ | 5.1g | 11.3g | ? | 4.6mg | 3.3mg |
(1)食物的成分主要有六大类营养素,上表中没有涉及的营养素是 ;
(2)假设该板栗中的钠元素以氯化钠的形式存在,则100g该板栗中,氯化钠的质量为mg(计算最后结果精确到0.1,下同);
(3)假设食物的热量是由蛋白质、糖类、油脂提供的,单位质量的蛋白质、糖类、油脂完全氧化放热约为:油脂 39.3kJ/g 蛋白质 18kJ/g 糖类 15.6kJ/g.根据此数据计算,理论上100g该板栗中油脂的质量为g.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对“某地爆炸事故”的调查发现:事故地存放有大量硝酸钾和碳化钙(CaC2).碳化钙遇水反应会生成乙炔(C2H2)和氢氧化钙,同时放出大量的热,乙炔是一种易燃的气体,它和空气混合极易爆炸.按所给信息回答问题:
(1)标出硝酸钾中氮元素的化合价.
(2)写出碳化钙与水反应的化学方程式.
(3)当失火地点存放有碳化钙时,可采用的灭火方法是什么?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com