
某化学兴趣小组为了分析生铁中铁的含量,进行了实验研究,即取60 g经粉碎后的生铁,把800稀硫酸分4次加入到该样品中,测得数据记录如下表:
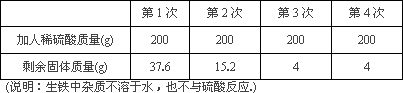
(1)第2次测得剩余固体质量为15.2 g,其成分为________.
A.铁
B.铁和碳
C.碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
(3)计算所用稀硫酸的溶质质量分数为多少?(写出计算过程,结果保留到小数点后一位)
并画出反应生成的氢气质量与加入稀硫酸质量的关系图.

答案:
(1)B (2)93.3% (3)19.6%
1、第二次剩余固体成分为:B铁和碳 。因为第一次200 g 只溶解(60- 37.6)g=22.4g铁,第二次也只溶解(37.6- 15.2 )g=22.4g铁,还剩生铁15.2g 2、800g稀盐酸分四次与60g生铁反应,从实验记录可看出第三次已完全反应,剩余固体质量为 4g。所以生铁中铁的质量分数为(60-4)/60×100%=93.3% 3、设硫酸质量为X,从实验记录第一次 、 第二次 数据可知:200 g 可溶解22.4g铁 Fe + H2SO4 = FeSO4 + H2 56 98 22.4 x x=39.2g 所用稀硫酸的溶质质量分数=39.2/200×100%=19.6%


科目:初中化学 来源: 题型:
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0 g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 每次加入盐酸量/g | 5.0 | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固体质量/g | 1.5 | 1.0 | 0.5 | 0.4 | 0.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com