写出下列反应的化学方程式:
(1)用高锰酸钾加热制取氧气;
(2)绿色植物的光合作用;
(3)铁丝与稀硫酸反应;
(4)氢氧化钙与盐酸反应.
上述反应中,属于分解反应的是;属于复分解反应的是.(填序号)
【答案】
分析:(1)用高锰酸钾加热制取氧气,反应物KMnO
4,生成物K
2MnO
4、MnO
2、O
2,反应条件加热,根据质量守恒定律,书写化学方程式;
(2)绿色植物的光合作用,反应物为CO
2、H
2O,生成物为C
6H
12O
6、O
2,反应条件为光照和在叶绿素,根据质量守恒定律,书写化学方程式;
(3)铁丝与稀硫酸反应,反应物Fe、H
2SO
4,生成物FeSO
4、H
2,根据质量守恒定律,书写化学方程式;
(4)氢氧化钙与盐酸反应,反应物Ca(OH)
2、HCl,生成物CaCl
2、H
2O,根据质量守恒定律,书写化学方程式;
①分解反应:指一种化合物在特定条件下(如加热,通直流电,催化剂等)分解成二种或二种以上较简单的单质或化合物的反应;可简记为AB=A+B;如碳酸分解生成二氧化碳和水,用高锰酸钾加热制取氧气;
②复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应;可简记为AB+CD=AD+CB;如氢氧化钠溶液与盐酸反应,
解答:解:(1)由题意,知反应物,生成物,反应条件,根据质量守恒定律,故书写化学方程式2KMnO
4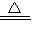
K
2MnO
4+MnO
2+O
2↑;
(2)由题意,知反应物,生成物,反应条件,根据质量守恒定律,故书写化学方程式6CO
2+6H
2O
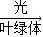
C
6H
12O
6+6O
2;
(3)由题意,知反应物,生成物,根据质量守恒定律,故书写化学方程式Fe+H
2SO
4═FeSO
4+H
2↑;
(4)由题意,知反应物,生成物,根据质量守恒定律,故书写化学方程式Ca(OH)
2+2HCl═CaCl
2+2H
2O;
①分解反应:符合AB=A+B,如用高锰酸钾加热制取氧气;
②复分解反应:符合AB+CD=AD+CB;如氢氧化钙与盐酸反应.
故答为:(1)2KMnO
4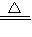
K
2MnO
4+MnO
2+O
2↑;
(2)6CO
2+6H
2O
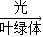
C
6H
12O
6+6O
2;
(3)Fe+H
2SO
4═FeSO
4+H
2↑;
(4)Ca(OH)
2+2HCl═CaCl
2+2H
2O;(1);(4)
点评:由题意,找出反应物和生成物、反应条件,正确书写化学方程式,掌握判定化学反应类型的方法.

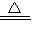 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;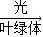 C6H12O6+6O2;
C6H12O6+6O2;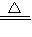 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;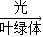 C6H12O6+6O2;
C6H12O6+6O2;