
| ||
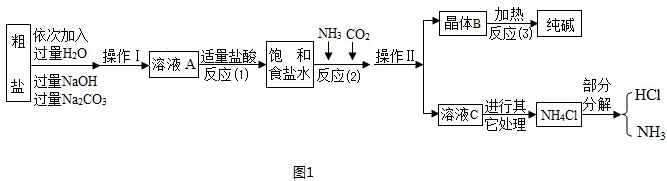
| 选择的装置(填序号) | 实验现象 | 实验结论 |
| 样品不含晶体B |
| ||
| 106 |
| x |
| 197 |
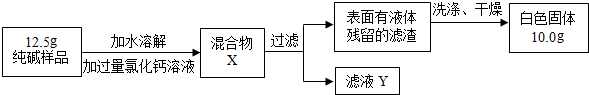
| 10.0g |
| 5.38g |
| 12.5g |
| ||
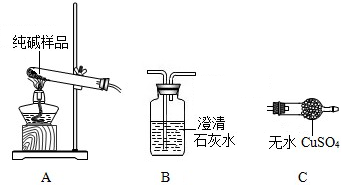
| 选择的装置 | 实验现象 | 实验结论 |
| AB或AC或ACB | B中不变浑浊,或C中不变蓝色,或C中不变蓝色且B中不变浑浊 | 样品不含晶体B |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| A、3 | B、2 | C、1 | D、0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量白色物质于试管中,加入适量水振荡,样品全部溶于水,向其加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示:请计算:(要求都写出计算过程)
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示:请计算:(要求都写出计算过程)查看答案和解析>>
科目:初中化学 来源: 题型:
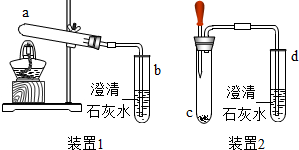 制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口.小明对泡打粉的发面原理产生兴趣,进行了以下实验探究.
制作馒头时常加入泡打粉,在制作过程中由于产生二氧化碳气体,使馒头变得松软可口.小明对泡打粉的发面原理产生兴趣,进行了以下实验探究.| 序号 | 实验方案 | 实验现象 | 实验结论 |
| Ⅰ | 在装置1的a试管中放入小苏打,加热 | a试管口内壁有无色液滴, | b试管中发生反应的化学方程式为 猜想1正确 |
| Ⅱ | 在装置1的a试管中放入酒石酸氢钾,加热 | a试管口内壁有无色液滴,石灰水不变浑浊 | |
| Ⅲ | 在装置2的c试管中放入小苏打和酒石酸氢钾的混合物,滴加 | 石灰水变浑浊 | 猜想3正确 |
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 化学与我们的身体健康和生产生活有着密切的关系.
化学与我们的身体健康和生产生活有着密切的关系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com