
 ��������Ϊ�ִ���ҵ�Ľ�ǣ���Ӧ����㷺�Ľ������ϣ�
��������Ϊ�ִ���ҵ�Ľ�ǣ���Ӧ����㷺�Ľ������ϣ����� ��1������������ԭ�����
��2���������غ㶨�ɣ���Ӧǰ��ԭ�����ࡢ��Ŀ�����䣬�ݴ��ɷ�Ӧ�Ļ�ѧ����ʽ�ƶϷ�Ӧ��Ļ�ѧʽ���ɷ�Ӧ����ȷ����Ӧ���ͣ�
��3���Ͻ�Ҫ��������Ĵ�������Ӳ�ȴ���
��4���ڽ������˳���У������⣾ͭ��������ǰ�Ľ��������ᷴӦ����������λ����ǰ�Ľ����ܽ�λ�����Ľ�����������Һ���û�������
��5�������������������������Ʒ����������������������������ͭ�����������Ʒ������ͭ������������
��� �⣺��1��������ԭ���ǡ���̿������ʯ��ʯ��ʯ��
��2�����ݷ�Ӧ�Ļ�ѧ����ʽ����δ֪��Ӧ��Ļ�ѧʽΪX��Ӧ��������������ԭ�Ӹ����ֱ�Ϊ4��10��8����Ӧ���������������������ԭ�Ӹ����ֱ�Ϊ4��12��12�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��2X����2����ԭ�Ӻ�4����ԭ�ӣ���ÿ��X����1����ԭ�Ӻ�2����ԭ�ӹ��ɣ�������X�Ļ�ѧʽΪH2O���÷�Ӧ���ϡ����һ�������������ڻ��Ϸ�Ӧ��
��3��������Ƭ������Ƭ����̻�����ͭƬ���������ԵĻ��ۣ�˵��������Ӳ�ȱȴ�����Ӳ�ȴ�
��4������Cu��NO3��2��AgNO3�ķ�Һ�м���һ������Al��Zn��������������������Ӧ��������������������������ͭ��Ӧ��������������ͭ�����ɵ�ͭ������������Ӧ��������ͭ����������������������ͭͬʱ����ʱ����������������������ͭ��Ӧ������Ӧ�꣬п����������������ͭ��Ӧ�������м���ϡ���ᣬ���������ݲ�������������һ������п��������ʣ���������������һ������п��ͭ��������Һ��һ��������������
��5������Ʒ��������������Ϊx
Fe+H2SO4 =H2��+FeSO4
56 2
x 0.4g
$\frac{56}{x}=\frac{2}{0.4g}$
x=11.2g
��Ʒ��������������$\frac{11.2g}{14.0g}$��100%=80%
����������ͭ��ȫ��Ӧ����������Ϊy��
Fe+CuSO4=FeSO4+Cu
56 64
y 6.4g
$\frac{56}{x}=\frac{64}{6.4g}$
y=5.6g
��a��$\frac{5.6g}{80%}$��100%=7g��
�ʴ�Ϊ��
��1����̿��
��2��H2O�����Ϸ�Ӧ
��3���Ͻ��Ӳ�ȱ���ֽ�����Ӳ�ȴ�
��4��Al��NO3��3��Zn��Cu��Ag��
��5��80%�� 7
���� �����˳���������п��ͭ�����Ľ������ǿ��������������˳�����Ӧ�ã����п����ȵ㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ʵ�鲽�� | ʵ������ | ʵ����� | |
| С�� | ȡ�����Թ��У����뼸��ϡ���� | û�����ݲ��� | ������������ |
| С�� | ȡ�����Թ��У�ͨ�������̼���� | �Թ��г��ְ�ɫ���� | �����ij��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ȼÿ�����������������ձ����ڻ����Ϸ� | ȼ�պ�Ѹ�ٷֱ����ձ���ע�����ʯ��ˮ | |
| A | �ձ�������ˮ�� | ʯ��ˮ����� |
| B | ������ | ʯ��ˮ����� |
| C | �ձ�������ˮ�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg��Al��Fe | B�� | Fe��Al��Mg | C�� | Al��Mg��Fe | D�� | Mg=Al=Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 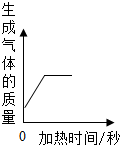 ����һ�������ĸ��������ȡ���� | |
| B�� | 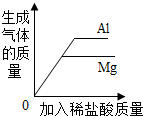 ���������Ǧ�ۺ�þ���зֱ��������������ͬ��������ϡ���� | |
| C�� | 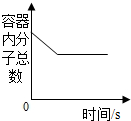 �����������������ܱ���������ȫ��Ӧ | |
| D�� |  ��һ���������Ȼ�����ϡ����Ļ����Һ����μ�������������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����õ�ȼ�ķ�����ȥ������̼�л��е�����һ����̼ | |
| B�� | ʯī���������ĵ������ܣ����������缫 | |
| C�� | �Ͻ�Ӳ��һ���������Ĵ������� | |
| D�� | ����粒�������ˮʱ���ȣ����������ƹ�������ˮʱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CuCl2��NaOH | B�� | NaCl��AgNO3 | C�� | NaOH��HCl | D�� | NaNO3��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com