
分析 【交流讨论】根据酸碱中和反应没有明显现象,需要借助酸碱指示剂才能判断反应是否发生进行分析;
【探究实验】根据硫酸根离子和钡离子会生成白色的硫酸钡沉淀进行分析;
根据铜离子和氢氧根离子会生成蓝色的氢氧化铜沉淀进行分析;
根据硝酸铜和氢氧化钠会生成氢氧化铜沉淀和硝酸钠进行分析;
根据检验硫酸根离子,用氯化钡和稀硝酸检验进行分析;
【反思与总结】根据用化学实验的方法验证同一溶液中两种物质的存在,不仅所加试剂与被检验物质能发生反应,还需要考虑所加试剂对另一种物质的检验不产生干扰进行分析.
解答 解:【交流讨论】酸碱中和反应没有明显现象,需要借助酸碱指示剂才能判断反应是否发生,所以小岗同学的方案不正确,理由是:氢氧化钠与盐酸反应无明显现象,无法确定溶液中是否含有氢氧化钠,由此得出结论,用化学实验的方法验证物质的存在,不仅所加试剂与被检验物质能发生化学反应,还需要有明显的实验现象,才能验证物质的存在;
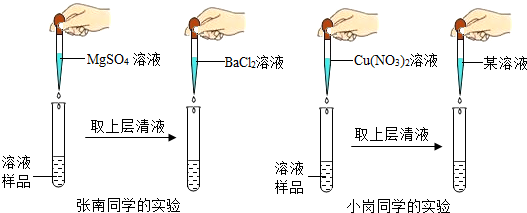
【探究实验】硫酸根离子和钡离子会生成白色的硫酸钡沉淀,所以张南同学的实验及结论不正确,理由是:加入硫酸镁产生白色沉淀,说明溶液中含有氢氧化钠存在是正确的,硫酸镁和生成的硫酸钠都能与氯化钡产生白色沉淀,无法证明硫酸钠的存在;
铜离子和氢氧根离子会生成蓝色的氢氧化铜沉淀,所以重新取溶液样品少许于试管中,其中滴加足量Cu(NO3)2 溶液,出现蓝色沉淀,硝酸铜和氢氧化钠会生成氢氧化铜沉淀和硝酸钠,化学方程式为:Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3;检验硫酸根离子,用氯化钡和稀硝酸检验,所以待上述沉淀完全后,取上层清液,再滴加氯化钡溶液和稀硝酸溶液,出现白色沉淀,可确定溶液中溶质含Na2SO4;
【反思与总结】用化学实验的方法验证同一溶液中两种物质的存在,不仅所加试剂与被检验物质能发生反应,还需要考虑所加试剂对另一种物质的检验不产生干扰,才能验证这两种物质的存在.
故答案为:【交流讨论】不正确,氢氧化钠与盐酸反应无明显现象,无法确定溶液中是否含有氢氧化钠,由此得出结论,有明显的实验现象;
【探究实验】不正确,加入硫酸镁产生白色沉淀,说明溶液中含有氢氧化钠存在是正确的,硫酸镁和生成的硫酸钠都能与氯化钡产生白色沉淀,无法证明硫酸钠的存在;
蓝色沉淀;Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3;氯化钡溶液和稀硝酸;
【反思与总结】对另一种物质的检验不产生干扰.
点评 本题主要考查了物质的检验,注意加入的试剂不能对另一种物质的检验造成干扰.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:选择题
| A. | 水$\stackrel{通电}{→}$氢气+氧气 | B. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | ||
| C. | 铝+氧气$\stackrel{点燃}{→}$氧化铝 | D. | 乙炔+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可以用明矾鉴定湘江水是硬水还是软水 | |
| B. | 大量使用农药、化肥,不会造成湘江水污染 | |
| C. | 湘江穿城而过,因而株洲人不需节约用水 | |
| D. | 在沉淀、过滤、蒸馏等湘江水的净化操作中,净化程度最高的是蒸馏 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com