
分析 根据假黄金的成分铜和锌的性质可知,加入稀硫酸时,只有锌与硫酸反应生成了硫酸锌和氢气;根据质量守恒定律,烧杯内质量的减少的质量即生成的氢气质量,据此根据反应的化学方程式列式计算出参加反应锌的质量、硫酸中溶质的质量,进而计算出铜的质量和铜的质量分数、所用稀硫酸的浓度.
解答 解:①根据质量守恒定律,产生氢气的质量为:10g+100g-109.8g=0.2g.
设黄铜样品中锌的质量为x,100g稀硫酸中溶质的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 98 2
x y 0.2g
$\frac{65}{2}=\frac{x}{0.2g}$ 解得:x=6.5g
$\frac{98}{2}=\frac{y}{0.2g}$ 解得:y=9.8g
黄铜样品中铜的质量分数为:$\frac{10g-6.5g}{10g}$×100%=35%.
②所用稀硫酸的浓度是:$\frac{9.8g}{100g}×100%$=9.8%.
答:①合金中铜的质量分数是35%;
②所用稀硫酸的浓度是9.8%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:实验探究题
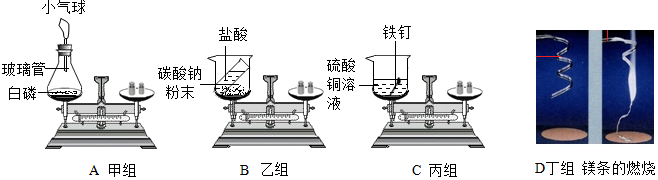
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
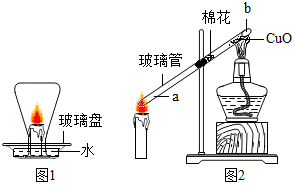
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事 实 | 解 释 |
| A | 一滴水中大约有1.67×1021个水分子 | 分子很小 |
| B | 敞口容器中的酒精逐渐减少 | 分子是不断运动的 |
| C | 体温计中的水银(汞)热胀冷缩 | 原子的体积热胀冷缩 |
| D | 炎热的夏天自行车车胎容易爆裂 | 夏天温度高,分子间隔变大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
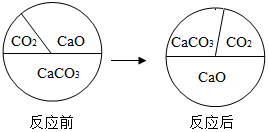 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )| A. | 反应中CaO为催化剂 | B. | 反应后容器中氧元素质量分数不变 | ||
| C. | 该反应是化合反应 | D. | 反应后容器中固体质量不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
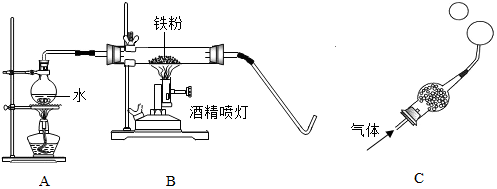
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量稀盐酸 | 无气泡产生,黑色固体是Fe3O4 |
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量∕g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
| 生成氢气的质量∕g | 0.2 | 0.2 | 0.2 | Y |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com