
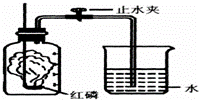
某同学设计了测定空气中氧气含量的实验,实验装置如图.
该同学的实验步骤如下:
①将图中的集气瓶分为5等份,并作好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷需稍过量,目的是 .
(2)步骤③中打开止水夹后观察到的现象是 ,由此可得出空气中氧气的体积分数约为 .
(3)实验过程中,观察到的主要现象是 , .反应的化学方程式是 .
| 空气组成的测定;书写化学方程式、文字表达式、电离方程式.. | |
| 专题: | 空气与水. |
| 分析: | (1)根据该实验注意事项分析; (2)根据红磷的燃烧现象、反应结合压强知识分析.红磷与氧气反应生成五氧化二磷固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶; (3)根据实验过程中观察到的主要现象,进行分析;根据化学方程式的书写方法进行回答. |
| 解答: | 解:(1)该实验中红磷需稍过量,目的是:确保将集气瓶内的氧气消耗尽; (2)点燃的红磷,在集气瓶燃烧,生成大量的白烟;由于红磷与氧气反应生成五氧化二磷固体,消耗了瓶内的气体,压强减小,所以,打开止水夹后观察到的现是:烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;由此可得出空气中氧气的体积分数约为五分之一. (3)步骤②集气瓶中的现象是:红磷燃烧放出大量白烟,发黄光,同时释放出大量的热;红磷燃烧生成五氧化二磷;由于红磷消耗了空气中的氧气使集气瓶内的压强减小,打开止水夹后观察到:烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;反应的化学方程式是4P+5O2 故答案为: (1)确保将集气瓶内的氧气消耗尽; (2)烧杯中的水倒流至集气瓶,液面上升在一等分刻度处; 五分之一. (3)红磷燃烧放出大量白烟,发黄光,同时释放出大量的热;烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;反应的化学方程式是4P+5O2 |
| 点评: | 本题考查学生对实验原理与实验操作的理解等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力. |


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:初中化学 来源: 题型:
九月走进颐和园大门,可闻到怡人的桂花香味,这﹣现象说明( )
|
| A. | 分子是由原子构成的 | B. | 分子分裂成原子 |
|
| C. | 分子在不断地运动 | D. | 分子之间有间隔 |
查看答案和解析>>
科目:初中化学 来源: 题型:
下列对分子、原子、离子的认识,正确的是( )
A. 原子是最小的粒子,不可再分
B. 温度越高,分子运动速率越快
C. 离子不能直接构成物质
D. 固体难压缩,说明固体分子间无间隔
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com