
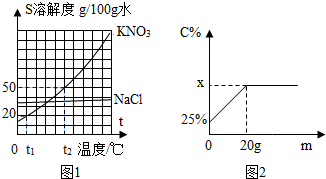
 如图1为KNO3和NaCl两种物质的溶解度曲线.
如图1为KNO3和NaCl两种物质的溶解度曲线.| 100g×25%+20g |
| 100g+20g |
| 20 |
| 120 |
| 50 |
| 150 |


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:初中化学 来源: 题型:
| 序号 | 化学反应事实 | 影响化学反应的因素 |
| A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
| C | 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
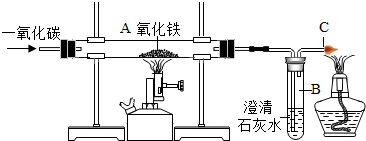
查看答案和解析>>
科目:初中化学 来源: 题型:
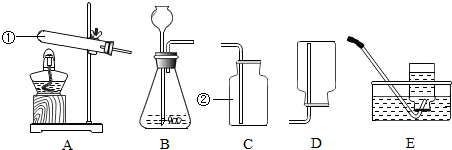
查看答案和解析>>
科目:初中化学 来源: 题型:
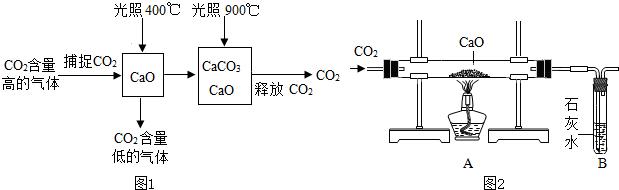
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取A中的固体少许加入足 量水中溶解,过滤. |
得到白色固体和无色溶液 | |
| ② | 取少量滤液于试管中,通 入 |
溶液变浑浊 | 固体中含有CaO |
| ③ | 取白色固体, |
白色固体是CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
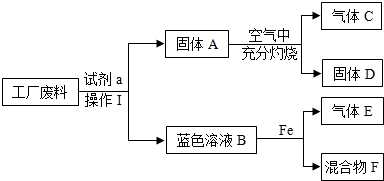 人类生产和生活中都离不开金属.
人类生产和生活中都离不开金属.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com