
现有①氢氧化钠②碳酸氢钠③食盐④氢氧化钙⑤食醋⑥硝酸铵等六种物质,选择适当的物质进行填空(填序号).
(1)澄清石灰水中的溶质是________;
(2)pH小于7的厨房调味品是________.
(3)炒菜常用的调味品是________;
(4)常应用于制取肥皂的碱是________.
(5)用作食品发酵粉的主要成分是________;
(6)一种常见的化学肥料是________.
④⑤③①②⑥ 【解析】 (1)澄清石灰水中的溶质是氢氧化钙,故填④; (2)食醋的pH小于7,pH小于7的厨房调味品是食醋,故填⑤; (3)炒菜常用的调味品是氯化钠,即食盐,故填③; (4)氢氧化钠是可应用于制取肥皂的碱.故填①; (5)用作食品发酵粉的主要成分是碳酸氢钠,故填②; (6)硝酸铵中含有氮元素,属于氮肥,是一种常见的化学肥料,故填⑥; ...科目:初中化学 来源:广东省2019届九年级化学:第二单元测试卷 题型:推断题
将一种无色无味的液体A装入试管,用带火星的木条伸入试管,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C且瓶底有少量液体D的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F。
(1)写出它们的名称:
A.______;B._______;C._______;D._______;E._______;F._______。
(2)黑色粉末B在A的分解反应中起_______。
(3)写出有关反应的文字表达式:_______;_______。
过氧化氢 二氧化锰氧气水铁四氧化三铁催化作用过氧化氢水+氧气铁+氧气四氧化三铁 【解析】 (1)C使带火星的木条复燃,故C为氧气,无色无味的液体A中加入少量黑色粉末B后,迅速产生氧气,根据氧气的制法可知A为双氧水,B为二氧化锰;金属E在氧气中剧烈燃烧,火星四射,生成黑色固体F,则E为铁,F为四氧化三铁;为防止铁丝燃烧时溅落的熔化物炸裂瓶底,集气瓶底要盛少量水,故D为水 (2)二氧...查看答案和解析>>
科目:初中化学 来源:广东省2019届九年级化学:第九单元测试卷 题型:科学探究题
仔细阅读下面的探究实验信息,回答相关问题。
Ⅰ.(实验目的)探究溶解过程中,溶液温度的变化情况。
Ⅱ.(查阅资料)
(1)物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
(2)实验条件下,水的凝固点为0 ℃、沸点为100 ℃。
Ⅲ.(提出猜想)物质溶解过程中,溶液的温度可能升高或降低或不变。
Ⅳ.(实验探究)某探究小组的同学设计了如下图所示的两种实验方案。在图2所示方案中,每次加入物质b之前,均使用温度计控制热水温度,使之保持在_____ ℃。
Ⅴ.(实验结论)图1所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度_____ (填“升高”“降低”或“不变”,下同)。图2所示实验中,若加入物质b后,热水会突然沸腾,说明_____。

Ⅵ.(拓展实验)按照图3所示进行实验。若物质c为NaOH,则U形管内的左边液面将_____ (填“高于”“低于”或“等于”)右边液面;若U形管内的液面位置变化与之相反,则物质c为_____ (填序号)。
①CaO ②NH4NO3 ③浓H2SO4
99降低溶液的温度升高低于② 【解析】 Ⅳ.【实验探究】由图中的条件可知:在图2所示方案中,每次加入物质b之前,均使用温度计控制热水温度,使之保持在99℃; Ⅴ.图1所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度下降; 图2所示实验中,若加入物质b后,热水会突然沸腾,说明溶液的温度升高; Ⅵ.若物质c为NaOH,氢氧化钠溶于水放热,装置内...查看答案和解析>>
科目:初中化学 来源:广东省2019届九年级化学:第九单元测试卷 题型:单选题
用浓盐酸配制一定溶质质量分数的稀盐酸,实验时必不可少的一组仪器是( )
A. 玻璃棒 量筒 烧杯 胶头滴管 B. 托盘天平 量筒 烧杯 玻璃棒
C. 托盘天平 玻璃棒 烧杯 胶头滴管 D. 量筒 烧杯 漏斗 玻璃棒
A 【解析】 试题A、配制定溶质质量分数的稀盐酸,用到的仪器有:玻璃棒 量筒 烧杯 胶头滴管,正确;B、不用托盘天平称量固体药品,错误;C、不用托盘天平称量固体药品,错误;D、不用漏斗,错误。故选A查看答案和解析>>
科目:初中化学 来源:沪教版九年级上册化学第七章应用广泛的酸、碱、盐 单元测试卷 题型:综合题
利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数. 下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.
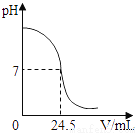
(1)根据下图曲线可以判断实验中是向________(填“酸”或“碱”,下同)溶液(待测液)中滴加________溶液(标准液).
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到________,则证明中和反应正好完成.
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计.若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数.
碱;酸碱溶液的红色刚好褪去3.6%. 【解析】 由图中溶液的pH变化情况,未加入时溶液的pH大于7,显碱性,后来溶液的pH逐渐减小,最终小于7,故开始是碱性溶液,过程中向碱溶液中滴加酸溶液,故填:碱,酸。 酚酞遇碱性溶液会变红,遇中性溶液不变色,中和反应刚好完成时溶液显中性,此时红色褪为无色,故填:碱溶液的红色刚好褪去。 设待测液溶质的质量分数为x, 2NaOH+H2...查看答案和解析>>
科目:初中化学 来源:沪教版九年级上册化学第七章应用广泛的酸、碱、盐 单元测试卷 题型:填空题
空气、水和土壤是人类赖以生存的自然资源,我们要保护它。
(1)由于森林的过量砍伐、草场大面积开垦,土地出现沙漠化,导致了沙尘暴。沙尘暴使空气中增加了大量的________ 。(填字母,下同)。
A.可吸入颗粒物 B.一氧化碳 C.二氧化氮 D.二氧化硫
(2)鱼类可在“水”中呼吸,是因为“水”中含有一定量的________ 。
A.氧原子 B.氧元素 C.氧气 D.氧分子
(3)在水的净化过程中,除去水中难溶性杂质的方法是________ ,自来水厂常用二氧化氯(ClO2)消毒,其中氯元素的化合价为________ 。
(4)在农业上用于改良酸性土壤的碱是________ 。
A;C 、D;过滤;+4;氢氧化钙 【解析】 沙尘暴指强风从地面卷起大量沙尘,使空气中增加了大量的可吸入颗粒物,故选A。 生命呼吸离不开氧气,鱼类可在“水”中呼吸,是因为“水”中含有一定量的氧气;氧气是由大量的氧分子构成的,故选C、D。 过滤能除去水中难溶性杂质;二氧化氯(ClO2 )氧元素的化合价为-2价,化合物中各元素的化合价的代数和为零,所以氯元素的化合价为+4。 ...查看答案和解析>>
科目:初中化学 来源:沪教版九年级上册化学第七章应用广泛的酸、碱、盐 单元测试卷 题型:单选题
钾肥能促进作物茎秆粗壮,增强对病虫害和倒伏的抵抗能力。下列物质中能用作钾肥的是( )
A. 尿素〔CO(NH2)2〕 B. 硝酸铵(NH4NO3)
C. 磷酸二氢钙〔Ca(H2PO4)2〕 D. 硫酸钾〔K2SO4〕
D 【解析】 考点定位本题的考点是常见化肥的种类和作用。含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。 解答过程判断属于哪种化学肥料,关键要看化肥中含N、P、K元素中的哪一种。若含N,则是氮肥;若含P,则是磷肥;若含K,则是钾肥;若含N、P、K元素中的两种或两种以上,则是复合肥。结合题意...查看答案和解析>>
科目:初中化学 来源:人教版九年级上册化学试卷-第7单元《燃料及其利用》单元测试 题型:填空题
有六种气体:①氧气 ②氢气 ③氮气 ④一氧化碳 ⑤二氧化碳 ⑥甲烷
选择填空:
(1)在空气所占体积分数最大的是 (填序号,下同);
(2)可用来制汽水的是 ;
(3)将成为一种重要的无污染新型燃料的是 ;
(4)在冶金工业用来使金属氧化物还原以制取某些金属的是 ;
(5)能与人体血液中血红蛋白结合的有毒气体是 ;
(6)充分燃烧时生成两种氧化物的是 。
(1)③ (2)⑤ (3)② (4)②④(5)④ (6)⑥ 【解析】 本题考查的是空气的成分及各成分的体积分数,二氧化碳的化学性质,一氧化碳的毒性,一氧化碳还原氧化铁,甲烷、乙醇等常见有机物的性质和用途。根据已有知识直接解答。 (1)在空气所占体积分数最大的是氮气; (2)可用来制汽水的是二氧化碳; (3)将成为一种重要的无污染新型燃料的是氢气; (4)在冶金工...查看答案和解析>>
科目:初中化学 来源:广东省2019届九年级化学第六单元测试卷 题型:简答题
小英同学为了测定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
实验 | 第一次 | 第二次 | 第三次 |
加入稀盐酸的量/mL | 25 | 25 | 25 |
生成气体的质量/g | 2.2 | m | 1.1 |
试求:
(1)m的值是 g.
(2)求该样品中碳酸钙的质量分数(保留一位小数).
(1)2.2g; (2) 83.3% 【解析】试题(1)根据记录数据可发现,第三次实验中加入盐酸还有二氧化碳放出,并且第三次实验中只放出1.1g二氧化碳,说明盐酸有剩余,所以在第三次实验中碳酸钙已经反应完,说明第一次和第二次实验中盐酸全部反应,放出二氧化碳的质量均为2.2g; (2)根据二氧化碳的质量求出该石灰石样品中碳酸钙的质量,进而求出该石灰石样品中碳酸钙的质量分数即可. 【...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com