
小红和化学研究性学习小组的同学一起做完课本上的观察活动“分子运动”的实验后,他们又设计了以下三个探究实验,以进一步探究分子的运动情况.请你加入该小组的探究活动,并回答下列问题.
实验Ⅰ:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞溶液,再向其中滴加浓氨水,小烧杯中的溶液变成红色.通过此实验,你能得出的结论有________.
实验Ⅱ:如图甲所示,小烧杯A内放浓氨水.小烧杯B内放滴有酚酞的蒸馏水.一段时间后,小烧杯B中产生的实验现象是________,产生这一现象的原因是________.
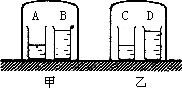
实验Ⅲ:为使实验结论可靠,他们又设计了如图乙所示的装置作为对比实验,小烧杯C中放入蒸馏水,小烧杯D中放滴有酚酞的蒸馏水.你认为有无必要?________,理由是________.
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:初中化学 来源: 题型:阅读理解
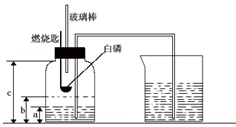 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:| b-a |
| c-a |
| 1 |
| 5 |
| b-a |
| c-a |
| 1 |
| 5 |
| 实验步骤 | 实验现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的氯化钙溶液,充分反应后过滤 | 产生白色沉淀 产生白色沉淀 |
有关反应的化学方程式为 Na2CO3+CaCl2=2NaCl+CaCO3↓ Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| 检验是否含有氢氧化钠 | 向过滤后的滤液中滴入 酚酞试液 酚酞试液 |
变红 变红 |
该样品中含有氢氧化钠 |
| 加入盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | 第七次 |
| 锥形瓶及所盛物质的总质量 | 95.00 | 120 | 145 | 170 | 192.8 | 215.6 | 240.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的氯化钙溶液, 充分反应后过滤 |
白色沉淀 白色沉淀 |
有关反应的化学方程式为 Na2CO3+CaCl2=2NaCl+CaCO3↓ Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| 检验是否含有氢氧化钠 | 向过滤后的滤液中滴入 酚酞试液 酚酞试液 |
变红 变红 |
该样品中含有氢氧化钠 |
| 106 |
| x |
| 44 |
| 4.4g |
| 10.6g |
| 16.40g |
| 106 |
| x |
| 44 |
| 4.4g |
| 10.6g |
| 16.40g |
| 加入盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | 第七次 |
| 锥形瓶及所盛物质的总质量 | 76.40 | 101.40 | 126.40 | 151.40 | 174.20 | 197.00 | 222.00 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
|
【查阅资料】:①白磷和红磷组成元素相同。白磷燃烧所需的
最低温度是40℃,而红磷需要240℃。
②紫色石蕊溶液是一种酸碱指示剂,酸性物质的溶液能使紫
色石蕊溶液变红。
【实验步骤】:
① 如右图所示连接仪器,检查装置的气密性良好。
② 在集气瓶里装入适量a体积的水,燃烧匙里放一块白磷,
在酒精灯上把玻璃棒下端加热后,立刻将集气瓶上的三孔胶塞塞紧。
③ 迅速将预热过的玻璃棒按下与白磷接触。观察到白磷燃烧,产生大量白烟。
④ 待白磷燃烧完毕,将集气瓶稍加振荡,白烟消失。
⑤ 待集气瓶完全冷却至室温,打开止水夹,量出集气瓶中水的体积为b,整个集气瓶的体积为c。
⑥ 根据a、b、c三个数据,计算出空气中氧气的体积分数。
根据以上实验信息,回答下列有关问题:
(1)为了充分 消耗容器中的氧气,药品中白磷的用量应保证 。
消耗容器中的氧气,药品中白磷的用量应保证 。
(2)若实验非常成功,请写出a、b、c三个数据应满足的一个等式关系 。
(3)小组成员小张对“实验前向集气瓶内装入适量a体积的水”不理解。咨询组长小明后,他终于明白加入水的作用,其一是 ;其二是 。
(4)小组成员小红无意间发现,向b体积水中滴加几滴紫色石蕊溶液,溶液会变成红色。请你对“变红”现象的原因提出大胆地猜想 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com