


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 钙 |
| 元素符号 | H | C | O | Cl | Na | Ca |
| ||
| ||
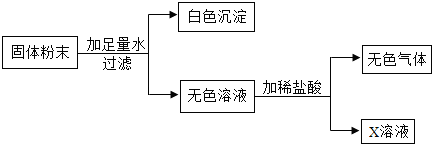
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
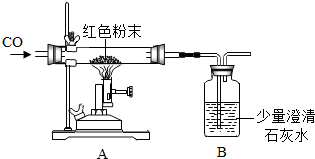 (2012?青岛模拟)现有一包干燥的红色粉末,它是由Cu、Fe2O3二种固体中的一种或两种组成,某化学兴趣小组对这包红色粉末的组成进行探究.请你参与并回答有关问题.
(2012?青岛模拟)现有一包干燥的红色粉末,它是由Cu、Fe2O3二种固体中的一种或两种组成,某化学兴趣小组对这包红色粉末的组成进行探究.请你参与并回答有关问题.| 反应前 | 反应后 | |
| Ⅰ 组 |
玻璃管和红色粉末的总质量为37g | 玻璃管和固体物质的总质量为34.6g |
| Ⅱ 组 |
洗气瓶B和所盛溶液的总质量为180.0g | 洗气瓶B和瓶中物质的总质量为181.1g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:2012年山东省青岛市中考调研化学试卷(解析版) 题型:解答题
| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为37g | 玻璃管和固体物质的总质量为34.6g |
| Ⅱ 组 | 洗气瓶B和所盛溶液的总质量为180.0g | 洗气瓶B和瓶中物质的总质量为181.1g |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com