
| A. | Na2O | B. | NaCl | C. | CuSO4﹒5H2O | D. | CaO |
分析 四种物质投入水中后,其中氧化钠与水反应生成氢氧化钠,氯化钠形成氯化钠溶液,CuSO4﹒5H2O溶于水后溶质为CuSO4,氧化钙与水反应生成为氢氧化钙,据此结合溶质质量分数=$\frac{溶质的质量}{溶液的质量}$×100%,进行分析解答.
解答 解:A、Na2O与水反应生成氢氧化钠,10克氧化钠与水反应生成的氢氧化钠的质量大于10g,而形成溶液的质量为10g+90g=100g;则最终所得溶液中溶质的质量分数大于10%;
B、氯化钠形成氯化钠溶液,将10克氯化钠投入到90克水中,最终所得溶液中溶质的质量分数为$\frac{10g}{10g+90g}$×100%=10%;
C、CuSO4﹒5H2O溶于水后溶质为CuSO4,10克CuSO4﹒5H2O与溶于水后溶质的质量小于10g,而形成溶液的质量为10g+90g=100g;则最终所得溶液中溶质的质量分数小于于10%;
D、氧化钙与水反应生成氢氧化钙,10克氧化钙与水反应生成的Ca(OH)2的虽质量大于10g,但由于Ca(OH)2的溶解度不超过0.2g,故能溶于水的Ca(OH)2还不足0.2g,形成溶液的质量为10g+90g=100g;则最终所得溶液中溶质的质量分数远小于10%;
对比四个选项可以看出,Na2O溶于水后所得溶液的溶质质量分数最大.
故选:A.
点评 此题是对溶质质量分数的考查,解题关键点是考虑10g物质放入水中时是否发生了变化,溶质种类与溶质的质量是否与所加入物质一致.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
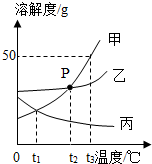 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
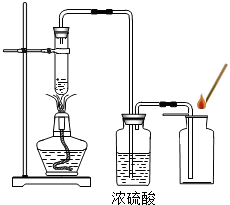 某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.
某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 液氧是混合物 | B. | 空气中氧气的体积分数约为21% | ||
| C. | 氧气的化学符号为O | D. | 含氧元素的物质是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com