
下列图象与对应实验相符合的是
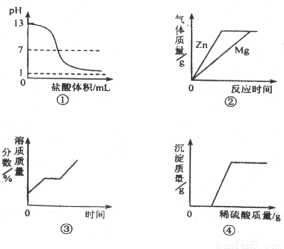
A.图①表示向pH=13的氢氧化钠溶液中逐滴加入pH=1的 盐酸
B.图②表示向溶质质量分数相同、等质量的稀硫酸中分别加入足量的金属镁和锌
C.图③表示将一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出
D.图④表示向氢氧化钠与氯化钡的混合溶液中逐滴加入稀硫酸
A 【解析】 试题分析:A、pH=13的氢氧化钠溶液中逐滴加入pH=1的盐酸发生中和反应,生成中性物质,碱性不断减弱至恰好反应时PH=7,再滴加盐酸酸性会不断增强,但不可能达到PH=1,故此选项正确;B、镁与锌是镁的活动性较强一些,加入盐酸时应该是镁反应较快,而图象是体现锌的速度快一些,故此选项错误;C、一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出的过程,是溶液由不饱和变成饱和的过程...科目:初中化学 来源:云南省昆明市业水平考试化学试卷 题型:单选题
一些常见物质的 pH 值如下,酸性最强的是( )
物质 | 牛奶 | 泡菜 | 肥皂 | 柠檬汁 |
物质 pH | 6.3 ~ 6.6 | 3.4 ~ 4.0 | 9.5 ~ 10.5 | 2.0 ~ 3.0 |
A. 牛奶 B. 泡菜 C. 肥皂 D. 柠檬汁
D 【解析】A、牛奶的pH为6.3 ~ 6.6,小于7,显酸性;B、泡菜的pH为3.4 ~ 4.0,小于7,显酸性;C、肥皂的pH为9.5 ~ 10.5,大于7,显碱性;D、柠檬汁的pH为2.0 ~ 3.0,小于7,显酸性。根据当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,柠檬汁的pH最小,酸性最强。故选D。故选A。查看答案和解析>>
科目:初中化学 来源:湖南省信阳市2018年中考模拟考试化学试卷 题型:填空题
某反应的微观示意图如图所示:

(1)该反应中化合价没变的元素是____。
(2)参加反应的甲物质和生成的丙物质分子数目比为____。
氢元素(或 H) 1:2 【解析】根据所学知识和题中信息知,(1)该反应中化合价没变的元素是氢元素(或 H),反应前是水,反应后是氟化氢,氢元素化合价没有变化。(2)根据质量守恒定律知, 2F2+2H2O=4HF+O2,参加反应的甲物质和生成的丙物质分子数目比为∶2∶4=1∶2。查看答案和解析>>
科目:初中化学 来源:湖南省信阳市2018年中考模拟考试化学试卷 题型:单选题
化学与生产、生活密切相关。下列说法不正确的是
A. 在铁制品表面刷漆可以防止生锈 B. 用灼烧法鉴别棉纱线和羊毛线
C. 回收废弃塑料能减少“白色污染” D. 煤气泄漏时打开抽油烟机排气
D 【解析】A、在铁制品表面刷漆可以防止生锈,在铁制品表面形成一层保护层,这是防止铁制品生锈措施之一,故A正确;B、用灼烧法鉴别棉纱线和羊毛线,羊毛线有一种烧焦的羽毛气味,故B正确;C、回收废弃塑料能减少“白色污染”, 废弃塑料是产生“白色污染”的主要原因,故C正确;D、煤气泄漏时不应打开抽油烟机排气,防止燃烧或爆炸,故D错误。 点睛∶刷漆是防止铁制品生锈措施之一,灼烧羊毛线有一种烧焦...查看答案和解析>>
科目:初中化学 来源:安徽省滁州市定远育才学校2018届九年级下学期期中考试化学试卷 题型:实验题
在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。
【实验目的】铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。

实验① 实验② 实验③
【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。
【实验结论】铁生锈实际上是铁与空气中的 (填名称)发生反应的结果。
【实验思考】
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 。
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 两种现象来判断铁丝反应进行的情况。
(3)铝比铁活泼,但铝难腐蚀,原因是 。
(4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议 。(答一点即可)
【实验结论】氧气和水蒸气 【实验思考】(1)1/5(21%)(2)试管内空气体积减小(或试管内液面上升) (3)易生成一层致密的氧化物保护膜,阻止铝不再被氧化 (4)回收利用(有计划合理地开采矿物;废旧金属的回收利用;寻找金属的替代品等合理答案均可) 【解析】试题分析:实验结论】铁在有水和氧气并存时易生锈,故填:氧气和水蒸气; 【实验思考】(1)铁丝足量,时间足够长,...查看答案和解析>>
科目:初中化学 来源:安徽省滁州市定远育才学校2018届九年级下学期期中考试化学试卷 题型:单选题
将10g质量分数为20%的氢氧化钠溶液与20g质量分数为10%的硫酸溶液混合后,下列物质中不能与该溶液发生反应的是( )
A. Na2CO3 B. CuCl2 C. CO2 D. Ba(NO3)2
A 【解析】【解析】 设参加反应的NaOH的质量为x, 2NaOH+H2SO4=Na2SO4+2H2O 80 98 x 20×10%g x≈1.63g<10g×20%, 故硫酸溶液被反应完,氢氧化钠溶液有剩余;所以反应后所得溶液中有NaOH和Na2SO4,它们与Na2CO3都含有钠元素,不能互相交换成分,故不能发生反应;A、由分析可知,所得溶液中有NaOH和N...查看答案和解析>>
科目:初中化学 来源:上海市奉贤区2018届九年级二模化学试卷 题型:科学探究题
为探究盐酸的化学性质,某同学做了如下实验:
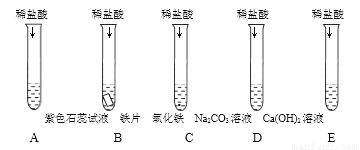
①A 中的现象是______;B 中反应的化学方程式为____;C 中反应原理的用途____;
②反应结束后,将 D、E 中的废液倒入同一个洁净的烧杯中,观察到先有气泡产生,后有白 色沉淀生成。过滤,得到白色沉淀和无色滤液。该同学欲探究无色滤液中的溶质。
无色滤液中一定不含 HCl,理由______(用化学方程式解释)。
【提出问题】无色滤液中的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl2;③NaCl和Na2CO3;④NaCl、CaCl2和Na2CO3。 你认为猜想______一定不正确?
【进行实验】
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想______成立 |
取少量滤液于试管中,滴加少量___ | 有气泡产生 |
查看答案和解析>>
科目:初中化学 来源:上海市奉贤区2018届九年级二模化学试卷 题型:单选题
互为同素异形体的是
A. 冰与干冰 B. 水与双氧水 C. 金刚石与石墨 D. 氧气与液氧
C 【解析】A、冰是水,干冰是二氧化碳,组成元素不同且都是化合物,错误;B、水和双氧水都属于化合物,错误;C、金刚石是由碳元素组成,石墨也是由碳元素组成,金刚石与石墨都是碳元素组成的不同单质,正确;D、液氧是液态的氧气,氧气和液氧是同一物质,错误。故选C。查看答案和解析>>
科目:初中化学 来源:北京市石景山区2018届初三一模化学试卷 题型:流程题
氯化钙应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产氯化钙的流程如下。
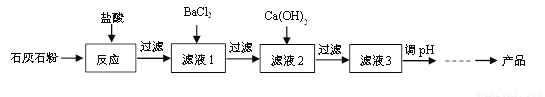
已知:BaCl2 + MgSO4 = BaSO4↓+ MgCl2
Ca(OH)2 + MgCl2 = Mg(OH)2↓+ CaCl2
Ca(OH)2 + FeCl3 = Fe(OH)3↓+ CaCl2
(1)氧化铁与盐酸反应的化学方程式为______。
(2)滤液1中的溶质有HCl、FeCl3、MgSO4和______。
(3)滤液2中加入Ca(OH)2是为了除去______(填序号,下同)。
A.MgCl2 B.FeCl3 C.HCl
(4)滤液3呈碱性,为使溶液pH降低,可加入适量的______。
A.NaCl B.NaOH C.盐酸
Fe2O3 + 6HCl = 2FeCl3 + 3H2O CaCl2 ABC C 【解析】(1)氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3 + 6HCl = 2FeCl3 + 3H2O;(2)碳酸钙和盐酸反应生成氯化钙、二氧化碳和水;(3)前两步中有盐酸,生成氯化镁、氯化铁,Ca(OH)2能将以上三种杂质除去;(4)盐酸显酸性,能降低溶液pH。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com