
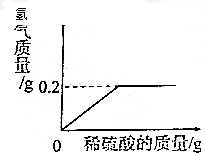
 取一定量9.8%的稀硫酸溶液与10g黄铜(含Zn和Cu)充分反应,反应的化学方程式为Zn+H2S04═ZnSO4+H2↑,有关量的变化如图所示.请回答:
取一定量9.8%的稀硫酸溶液与10g黄铜(含Zn和Cu)充分反应,反应的化学方程式为Zn+H2S04═ZnSO4+H2↑,有关量的变化如图所示.请回答:分析 (1)根据图可知生成氢气的质量即可;
(2)根据氢气的质量求出锌的质量,进而求出铜的质量以及黄铜中Cu的质量分数即可;
(3)根据氢气的质量求出生成硫酸锌的质量,进而求出反应后所得溶液的溶质质量分数.
解答 解:(1)根据图可知生成氢气的质量为0.2g;故填:0.2g;
(2)设黄铜中锌的质量为x,消耗硫酸溶液的质量为y,生成硫酸锌的质量为z.
Zn+H2SO4═ZnSO4+H2↑
65 98 161 2
x y×9.8% z 0.2g
$\frac{65}{x}=\frac{98}{y×9.8%}=\frac{2}{0.2g}$
x=6.5g
y=100g
z=16.1g
黄铜中Cu的质量分数=$\frac{10g-6.5g}{10g}×100%$=35.0%
铜难溶于水,所以可用过滤的方法分离出来;故填:35.0%;过滤;
(3)反应后所得溶液的溶质质量分数=$\frac{16.1g}{100g+6.5g-0.2g}×100%$=15.1%
答:反应后所得溶液的溶质质量分数为15.1%.
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 化学小组同学为了测定某工厂生产的小苏打中碳酸氢钠的质量分数(其中含有少量氯化钠),进行了以下实验,请根据实验过程和提供的数据进行计算:
化学小组同学为了测定某工厂生产的小苏打中碳酸氢钠的质量分数(其中含有少量氯化钠),进行了以下实验,请根据实验过程和提供的数据进行计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com