
| ʵ�鲽�� | ʵ������ | ���� |
| 1��ȡ��������Һ���Թ��У�������������Һ�� | �������ȷ | |
| 2������������Һ��ȡ�ϲ���Һ��������һ֧�Թ��У����뼸����Һ |
���� �����롿�������е�֪ʶ���з���������¶���ڿ���������Dz����ʡ����ֱ��ʻ��Dz����ʷ�����
������ʵ�顿��֤��Һ���ֱ��ʣ���Ҫ֤�����������ƣ���Ҫ֤����̼���ƽ��з�����̼�����ܹ����Ȼ�������Һ���������Ⱦ����������Ʊ��ʳ�̼���ƣ����ܹ���ȥ̼���Ƽ��Զ��������Ƶĸ��ţ��ٵμӷ�̪��Һ�۲��ɫ��ȷ����Һ����ɣ�
����˼�����������������ն�����̼����̼���ƺ�ˮ��
��� �⣺�����롿��������¶���ڿ���������Dz����ʡ����ֱ��ʻ��Dz����ʣ����ȫ�����ʣ�
������ʵ�顿����Һ����Ʒ�еμ��Ȼ�����Һ�������Ȼ�����̼���Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ����۲쵽�г������ֿ��жϱ���������̼���ƣ��ڷ�Ӧ�����Һ�е����̪����������������ʹ��̪��죬�����ֱ������ж����������ƣ���˼ȳ��ֳ���������Һ��죬����Һ���ֱ��ʣ����������ɣ����ʴ�Ϊ��
| ʵ�鲽�� | ʵ������ | ���� |
| 1��ȡ��������Һ���Թ��У��� �������Ģ�BaCl2��CaCl2��Ba��NO3��2����Һ�� | �а�ɫ���� | �������ȷ |
| 2������������Һ��ȡ�ϲ���Һ��������һ֧�Թ��У����뼸�� �ܷ�̪��Һ����ɫʯ����Һ����Һ | ����Һ��죨��Һ������ |
���� ���⿼���˾��õ�NaOH�����Ƿ���ʵ�ʵ��̽����ѧ����ȷʵ����������۵Ĺ�ϵ����ע�������ʵ�����������������ʵ�ԭ��������⣮��������������̼���ƵĻ����ʱ�����Ȱ�̼���Ʊ�ɳ������Ҳ�����Ӱ���������Ƽ���ļ������ʣ�Ȼ��ʹ�÷�̪�����������ƣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ҿ���ɵĸֱʼ�þ����ã�����������ҿ��Ԫ�����ڱ����й���Ϣ��ͼ������˵������ȷ���ǣ�������
��ҿ���ɵĸֱʼ�þ����ã�����������ҿ��Ԫ�����ڱ����й���Ϣ��ͼ������˵������ȷ���ǣ�������| A�� | ҿԪ�����ڽ���Ԫ�� | B�� | ҿ��ѧ���ʺ��ȶ� | ||
| C�� | ҿԭ�ӵĺ��������Ϊ77 | D�� | ҿԪ�ص����ԭ������Ϊ192.2g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͭ�ͻƽ�--���� | B�� | ��������غ��Ȼ���--ˮ | ||
| C�� | ������þ���Ȼ���--ϡ���� | D�� | �ȹ������Ϻ�����������--���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ռ��Ƿ���� | B�� | ��������ˮ���Ƿ��������� | ||
| C�� | ֤���������ﺬ��̼���� | D�� | ������Ǻʹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �ڷ��������һ������ֱ����ͭƬ��пƬ����Ϊ���ѵ�أ���ͭƬ��пƬ���ѹ����������ͼ��ʾ������˵����ȷ���ǣ�������
�ڷ��������һ������ֱ����ͭƬ��пƬ����Ϊ���ѵ�أ���ͭƬ��пƬ���ѹ����������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | п�缫�Ƿ��ѵ�ص����� | |
| B�� | ���ѵ�ؿɽ���ѧ��ת��Ϊ���� | |
| C�� | ���ѵ���γ�ͨ·���ӽ�ͭ�缫���� | |
| D�� | ����ѹ��ֱ�ӽ��ڸ÷��ѵ���ϣ�����ѹ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
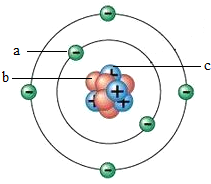 ͼΪijԭ�ӽṹģ�͵�ʾ��ͼ������a��b��c�ǹ��ɸ�ԭ�ӵ����ֲ�ͬ���ӣ�����˵����ȷ���ǣ�������
ͼΪijԭ�ӽṹģ�͵�ʾ��ͼ������a��b��c�ǹ��ɸ�ԭ�ӵ����ֲ�ͬ���ӣ�����˵����ȷ���ǣ�������| A�� | ������ԭ�������������b | B�� | ԭ����b��c����Ŀһ����ͬ | ||
| C�� | ԭ����a��c����Ŀһ����ͬ | D�� | ԭ�ӵ�����������a��c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/g/L | 63.7 | 28.8 | 144.6 | 46.4 |

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com