
【题目】近年各大体坛赛事报道频繁出现一个名词“嗅盐”。校兴趣小组在老师的指导下,对“嗅盐”展开了系列探究:
(查阅资料)①嗅盐,是一种由碳酸铵和香料配制而成的药品,给人闻后有刺激作用;
②嗅闻原理是碳酸铵晶体产生的氨气对人体有刺激作用,过量嗅闻不利健康;
③碳酸铵[(NH4)2CO3]晶体受热易分解,产生 NH3、H2O、CO2。
(定性初探)验证“嗅盐”的化学性质
(1)甲同学进行了NH4+的验证实验:取适量嗅盐于试管中,加入氢氧化钠溶液共热,在试管口放一张_____,观察到了预期的实验现象。请写出氢氧化钠溶液与碳酸铵反应的化学方程式_____。
(2)乙同学进行了 CO32﹣的验证实验:取适量嗅盐于试管中,再加入稀硫酸,并将生成的气体通入_____,预期的实验现象是_____,实验后观察到了预期的现象。
(定量再探)测定“嗅盐”中碳酸铵(NH4)2CO3的质量分数
方案Ⅰ:取样品 6.0 克,用图 1 装置进行实验,测量C装置在反应前后增加的质量即为产生NH4+的质量:
(3)装置B的作用_____,装置C中普通漏斗的作用是_____,图2装置中不能与其起到相似作用的是_____。
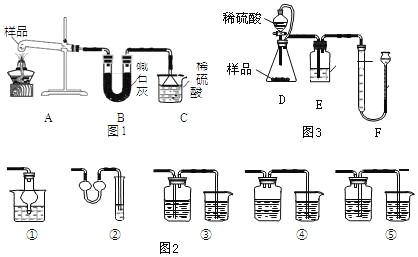
(4)小组同学经讨论后,均认为用该套装置测量会导致碳酸铵的质量分数偏小,原因是_____。
方案Ⅱ:取样品6.0克,用图3装置进行实验,利用F装置测量反应生成气体的体积。
(5)请写出装置D中发生反应的化学方程式_____,装置 D 中橡胶管除平衡压强,便于液体顺利滴下外,还有_____的作用。
(6)该方案实验结束后,会有气体残留,不能完全进入量气管中,_____(填“需要”或“不需要”)通入N2将其 中残留的气体排入量气管中,阐述你的理由_____。
(7)实验测得量气管中产生气体的体积为 558mL,该方案所测嗅盐中碳酸铵的质量分数为_____。
(已知实验条件下,CO2的密度约为 1.97g/L)。(请写出过程,计算结果精确到 1%)
(8)若其他操作均正确,下列因素会导致所测嗅盐中碳酸铵的质量分数偏大的是_____ (填字母)
a.反应前量气管液面在 0 刻度处以下
b.实验结束后,调节两端液面相平读数
c.反应结束后未等装置冷却到室温,就开始读数
【答案】湿润的红色石蕊试纸 (NH4)2CO3+2NaOH![]() Na2CO3+2H2O+2NH3↑ 澄清石灰水中 澄清石灰水变浑浊 吸收水和二氧化碳 防止液体倒吸入B中 ⑤ 生成的气体不能被完全吸收 (NH4)2CO3+H2SO4═(NH4)2SO4+H2O+CO2↑ 防止收集气体偏大 不需要 反应生成多少体积的气体,就有多少体积的气体进入量气管中 40% c
Na2CO3+2H2O+2NH3↑ 澄清石灰水中 澄清石灰水变浑浊 吸收水和二氧化碳 防止液体倒吸入B中 ⑤ 生成的气体不能被完全吸收 (NH4)2CO3+H2SO4═(NH4)2SO4+H2O+CO2↑ 防止收集气体偏大 不需要 反应生成多少体积的气体,就有多少体积的气体进入量气管中 40% c
【解析】
(1)取适量嗅盐于试管中,加入氢氧化钠溶液共热,在试管口放一张湿润的红色石蕊试纸,观察到了预期的实验现象,即湿润红色石蕊试纸变蓝色,故填湿润的红色石蕊试纸;
氢氧化钠溶液与碳酸铵在加热条件下反应生成碳酸钠、水和氨气,故反应的化学方程式写为:(NH4)2CO3+2NaOH![]() Na2CO3+2H2O+2NH3↑。
Na2CO3+2H2O+2NH3↑。
(2)取适量嗅盐于试管中,再加入稀硫酸,并将生成的气体通入澄清石灰水中,故填澄清石灰水中;预期的实验现象是澄清石灰水变浑浊,实验后观察到了预期的现象,故填澄清石灰水变浑浊。
(3)由图可知,装置 B 的作用吸收水和二氧化碳,故填吸收水和二氧化碳;
氨气极易溶于水,装置 C 中普通漏斗的作用是防止液体倒吸入B中,故填防止液体倒吸入B中;
下列装置中不能与其起到相似作用的是⑤,故填⑤。
(4)小组同学经讨论后,均认为用该套装置测量会导致碳酸铵的质量分数偏小,原因是生成的气体不能被完全吸收,故填生成的气体不能被完全吸收。
(5)装置 D 中碳酸铵和稀硫酸反应生成硫酸铵、水和二氧化碳,故反应的化学方程式写为:(NH4)2CO3+H2SO4═(NH4)2SO4+H2O+CO2↑;
装置 D 中橡胶管除平衡压强,便于液体顺利滴下外,还有防止收集气体偏大的作用,这是因为有多少体积的液体进入锥形瓶,就有多少体积的气体进入分液漏斗中,故填防止收集气体偏大。
(6)不需要通入N2将其中残留的气体排入量气管中,故填不需要;
理由是反应生成多少体积的气体,就有多少体积的气体进入量气管中,故填:反应生成多少体积的气体,就有多少体积的气体进入量气管中。
(7)解:反应生成二氧化碳质量:1.97g/L×0.558L=1.1g
设样品中碳酸铵质量为x
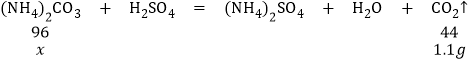
96:44=:1.1g
x=2.4g
嗅盐中碳酸铵的质量分数为:![]() ×100%=40%
×100%=40%
答:嗅盐中碳酸铵的质量分数为40%。
(8)a.反应前量气管液面在 0 刻度处以下,会导致读取的二氧化碳体积偏小,从而导致质量分数偏小;
b.实验结束后,调节两端液面相平读数,是正确的操作方法,不能导致实验结果偏大或偏小;
c.反应结束后未等装置冷却到室温,就开始读数,会导致二氧化碳体积偏大,从而导致质量分数偏大;故填c。


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源: 题型:
【题目】某化学自主学习小组为了测定某石灰石中碳酸钙的质量分数,取16g石灰石样品,加入适量的稀盐酸,恰好完全反应。有关数据如表所示(样品中其他成分均不与稀盐酸反应且不溶于水):
反应前 | 反应后 | ||
实验数据 | 石灰石样品的质量 | 加入稀盐酸的质量 | 剩余溶液的质量 |
16g | 30g | 41.6g | |
(1)完全反应时生成气体的质量为_____,完全反应后所得溶液中溶质的质量为_____。
(2)该石灰石样品中碳酸钙的质量分数?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F是初中化学常见的物质,A、B是含有相同元素的无色液体,D是最轻的气体,F是红色固体单质。根据如图的相互转化关系判断(图中反应条件及部分反应物、生成物已省略)。
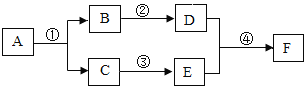
(1)F物质是___(填化学式)。
(2)写出反应①的化学方程式___。
查看答案和解析>>
科目:初中化学 来源: 题型:
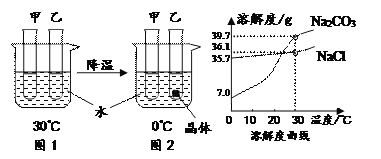
【题目】甲、乙试管中各盛有10.0g水,向其中一支试管中加入3.0g Na2CO3粉末,另一支试管中加入3.0gNaCl粉末,按图1、2进行实验。下列说法正确的是
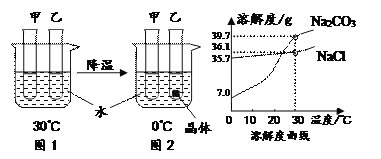
A. 甲中加入的粉末是Na2CO3
B. 0℃时,甲中溶液一定不饱和,乙中溶液一定饱和
C. Na2CO3中含有少量NaCl,可用冷却热饱和溶液的方法提纯Na2CO3
D. 30℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙试管中各盛有10.0g水,向其中一支试管中加入3.0g Na2CO3粉末,另一支试管中加入3.0gNaCl粉末,按图1、2进行实验。下列说法正确的是
A. 甲中加入的粉末是Na2CO3
B. 0℃时,甲中溶液一定不饱和,乙中溶液一定饱和
C. Na2CO3中含有少量NaCl,可用冷却热饱和溶液的方法提纯Na2CO3
D. 30℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请用化学用语回答生活中的下列问题。
(1)新鲜的苹果切开后因亚铁离子被氧化会很快变黄,亚铁离子的符号是______。
(2)工业盐因含亚硝酸钠(NaNO2)而有毒,标出亚硝酸钠中氮元素的化合价______。
(3)小苏打既可作发酵粉又可治疗胃酸,写出小苏打的化学式_____。
(4)某学习小组在帮助清理药品时,发现一瓶标签残缺盛有无色溶液(初中化学常用试剂)的试剂瓶(如图),你猜想这种试剂可能是____溶液。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量含CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示(不考虑二氧化碳气体的溶解)。下列说法正确的是( )
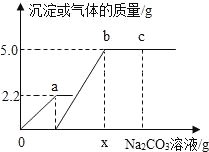
A. 图中 0~a段表示生成沉淀的过程
B. b点时,溶液中溶质有2种
C. c点时,溶液的pH=7
D. x值等于106.0
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元明粉(Na2SO4)常用于配制印染织物的促染剂,其溶质的质量分数一般在3%-5%范围。
(1)元明粉中钠、硫元素的质量比为_____。(写出最简整数比)
(2)配制1000g溶质的质量分数为4%的促染剂,需要_____mL(保留到小数点后一位)溶质质量分数为20%的硫酸钠溶液,需要水的质量为_____g。(已知常温下溶质质量分数为20%的硫酸钠溶液密度为1.2g/cm3)
(3)将某促染剂逐滴滴入100g氯化钡溶液中,恰好完全反应后过滤,洗涤干燥后得滤渣质量为8g。而氯化钡是由木炭在高温下还原重晶石(主要成分BaSO4)得到BaS,向其中再加入盐酸发生复分解反应而得到的。
①写出硫化钡与盐酸反应生成一种气体的化学方程式_____。
②通过滤渣质量计算需要这种含杂质20%的重晶石_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组按下图实验测定部分变质的Na0H固体中Na2CO3的质量分数。

(1)根据题中信息_______(填“能”或“不能”)计算Ca(OH)2溶液的溶质质量分数。
(2)计算固体混合物中Na2CO3的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com