
| A. | 紫色石蕊试液 | B. | 无色酚酞试液 | C. | pH试纸 | D. | 蓝色石蕊试液 |
分析 根据溶液酸碱度是溶液酸碱性的强弱程度,根据溶液酸碱度的测定方法,进行分析解答即可.
解答 解:酸碱指示剂和pH试纸都可以测溶液的酸碱性;溶液的酸碱度是指溶液的酸碱性强弱程度,一般用pH值来表示.溶液的酸碱度测定最简单的方法是使用pH试纸,利用石蕊试液、酚酞试液等酸碱指示剂只能判断溶液的酸碱性,不能测定溶液的酸碱度.
A、石蕊试液只能判断溶液的酸碱性,不能测定溶液的酸碱度,故选项错误.
B、酚酞试液只能判断溶液的酸碱性,不能测定溶液的酸碱度,故选项错误.
C、pH试纸是鉴别一瓶溶液的酸碱度的最简单的方法,故选项正确.
D、蓝色石蕊试液只能判断溶液的酸性,不能测定溶液的酸碱度,故选项错误.
故选:C.
点评 本题难度不大,掌握溶液酸碱度与酸碱性的区别、测定溶液酸碱度的方法是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验序号 | 水的质量/g | 所加NaCl的质量/g | 所得溶液的质量/g |
| ① | 100 | 20 | 120 |
| ② | 100 | 30 | 130 |
| ③ | 100 | 40 | 136 |
| ④ | 100 | 50 | 136 |
| A. | ①②所得溶液是20℃时NaCl的饱和溶液 | |
| B. | 20℃时,NaCl的溶解度为36g | |
| C. | ①②③所得溶液是20℃时NaCl的不饱和溶液 | |
| D. | ①所得溶液的溶质质量分数为20% |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
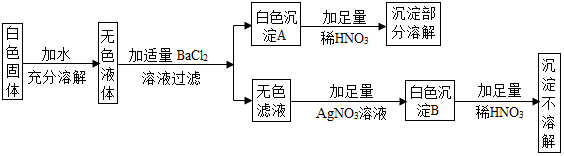
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 反应中产生的氧气质量为9.6g | B. | 反应中产生的氧气质量为5.6g | ||
| C. | 18.9g残余物全部是氯化钾 | D. | 18.9g的残余物中含有4g MnO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 用10mL的量筒量取9.0mL水 | |
| B. | 用排水法收集的氧气较纯净 | |
| C. | 用托盘天平称取10.58 g碳酸钠粉末 | |
| D. | 酒精灯不慎打翻起火,用水浇灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
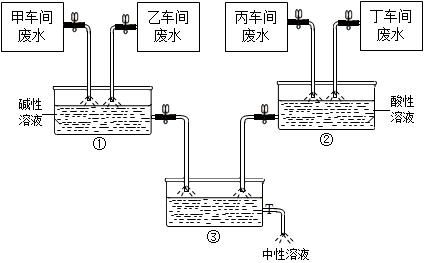 合理化处理废水是当前防治废水中的有害或有毒物质对环境造成污染的重要举措.某化学试剂厂甲、乙、丙、丁四个车间排放的废水中,主要成分分别含有CuCl2、HCl、Na2CO3、NaOH的一种.甲车间的废水呈蓝色.通过调节废水流量,使乙、丁两个车间废水相对过量,最终排出的废水呈中性.处理过程如图所示,在第①反应池中出现大量的蓝色沉淀,在第②反应池中出现大量的气泡.请回答:
合理化处理废水是当前防治废水中的有害或有毒物质对环境造成污染的重要举措.某化学试剂厂甲、乙、丙、丁四个车间排放的废水中,主要成分分别含有CuCl2、HCl、Na2CO3、NaOH的一种.甲车间的废水呈蓝色.通过调节废水流量,使乙、丁两个车间废水相对过量,最终排出的废水呈中性.处理过程如图所示,在第①反应池中出现大量的蓝色沉淀,在第②反应池中出现大量的气泡.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com